Ⅰ. 서 론
대상포진은 수두에 감염된 과거력이 있거나 수두 예방 접종을 받은 사람의 감각신경절에 잠복하고 있던 varicella-zoster virus(VZV)가 숙주 면역 체계의 변화로 재활성화되어, 해당 감각신경절이 지배하는 피부 분절에 편측성으로 수포성 발진과 통증을 일으키는 바이러스성 피부 질환이다1,2). 대상포진의 재발에는 숙주의 면역 상태가 가장 중요하나, 최근에는 고령의 나이, 외상, 당뇨, 고혈압, 이상지질혈증, 만성폐쇄성폐질환, 우울증, 갑상선기능저하증과 같은 만성질환도 대상포진의 발병 및 재발에 관여하는 것으로 보고되었다3-5). 그중에서 당뇨는 T세포의 기능 실조를 유발하여 대상포진과 대상포진 후 신경통의 발병률을 높이는 것으로 알려졌으며6-8), 이상지질혈증의 경우에는 높은 콜레스테롤 수치 또는 스타틴계 약물의 투여가 VZV의 재활성화를 유발하는 것으로 보고되었다9,10).
한의학에서는 ‘纏腰火丹’이라고 하여 원인은 肝經火盛, 脾經濕熱, 氣滯血瘀 등으로 보았고, 病因에 따라 龍膽瀉肝湯, 除濕胃笭湯, 逍遙散과 같은 처방을 사용해 왔다1). 대상포진의 한방 치료에 대한 증례 연구 논문은 최근까지 36편 이상 보고되어 있으며, 2000년 이후 평균적으로 매년 2편씩 증례 연구가 꾸준히 보고되고 있다11). 그러나 최근 10년 동안 수두 또는 대상포진의 과거력이 있는 경우는 1례12)밖에 확인되지 않았다.
우리나라는 2021년 2월 26일부터 코로나바이러스감염증-19(COVID-19) 백신 접종을 시작하였다. 미국과 영국에서 COVID-19 백신의 긴급 사용 승인을 위한 임상시험 결과, 대부분 가벼운 국소 이상 반응이 흔하게 나타났으며, 이마저도 접종 후 수일 이내에 소실되어13-15) 그 안전성이 입증되었다. 그럼에도 불구하고 COVID-19 백신 접종이 시작된 이후로 국내 및 해외에서 백신 접종 후 발생한 이상 반응은 꾸준히 보고되고 있으며, 가장 흔한 부작용으로는 두통, 접종 부위의 근육통, 어지러움 순으로 보고되어 있다16). 한편 본 증례에서처럼 COVID-19 백신 접종 후 대상포진이 재발한 사례는 해외에서는 이미 보고된 바 있으나, 국내에서는 아직 유사 증례 보고가 출판되지 않았다.
따라서 본 연구자들은 COVID-19 백신을 접종받은 후 대상포진이 재발하여 나주동신대학교 한방병원 한방안이비인후피부과에서 입원 치료를 받은 환자 1례를 대상으로 침 치료, 한약 치료, 紫河車 약침 시술 등의 한방 치료와 양방 치료를 병행하여 유의한 효과를 보였기에 보고하고자 한다.
Ⅱ. 증 례
-
환자 정보 : 박○○(F/42)
-
주소증 및 초진 소견
-
1) 오른손의 수포와 통증
上肢部의 병변은 오른손 손등쪽면에 분포하였다. 첫째손가락뼈사이관절(first interphalangeal joint), 둘째원위손가락뼈사이관절(second proximal inter-phalangeal joint) 및 둘째손허리손가락관절(second metacarpophalangeal joint), 陽谿穴(LI5)에서 偏歷穴(LI6)에 이르는 아래팔 부위에 각각 1-2개 정도의 수포가 산재되어 있었다. 수포는 대부분 이미 潰破되고 瘡面이 미란된 상태였으나, 일부 수포는 潰破되지 않은 상태였다. 수포로부터 흘러나온 것으로 보이는 삼출액은 관찰되지 않았다. 한편 셋째 및 넷째근위손가락뼈사이관절(third and fourth distal interphalangeal joints)와 두 손가락의 손허리뼈(metacarpal bone) 사이에는 수포 없이 홍반만 존재하였다. 환자는 환부의 주요 자각 증상으로 소양감을 호소하였으며, 발병 초기에는 통증이 심하였으나 내원 당시에는 열감이나 통증은 완화된 상태라고 하였다.
-
2) 우측 얼굴의 수포와 통증
대상포진으로 인한 피부 병변은 오른손뿐만 아니라 우측 얼굴에도 발생하였다. 얼굴에서는 입술 양측의 口角을 중심으로 하는 일대의 홍반과 부종이 관찰되었다. 홍반 표면에는 미세한 白色 鱗屑과 黃色 痂皮가 산재되어 있었다. 본원 입원 당일에는 얼굴의 수포는 이미 소실된 상태였다. 환자는 환부의 자각 증상으로 소양감과 열감을 호소하였으며, 통증은 오른손과 마찬가지로 발병 초기에는 심하였으나 현재는 완화된 상태라고 하였다.
-
-
발병일 : 2021년 8월 20일
-
진단명
-
현병력
본 환자는 2021년 7월까지 2차례의 대상포진 관련 과거력이 있는 분으로, 2021년 8월 16일에 화이자 社의 COVID-19 백신으로 1차 접종을 받고 2021년 8월 20일 상기 주소증 1, 2가 발생하여 2021년 8월 22일 영암한국병원 응급실 및 2021년 8월 23일 로컬 의원에서 두드러기로 진단받고 주사 및 약물 치료를 받았다. 그러나 증상이 호전되지 않고 심화되어 2021년 영암한국병원 내과에 내원하여 대상포진으로 진단받고 주사 및 약물 치료를 받았으며, 2021년 8월 24일에는 본원 한방안이비인후피부과에 내원하여 입원하였다.
-
과거력
-
1) 고혈압(-), 당뇨(-), 결핵(-), 간염(-)
-
2) 2010년경 건강검진에서 EGD상 만성 표재성 위염 Dx. no-tx.
-
3) 2010년경 로컬 병원 정형외과에서 L-spine MRI상 척추전방전위증 Dx. PTx. 이후 2015년경 동일 병원에서 신경차단술-tx.
-
4) 2016년경 신체 우측면(구체적인 발병 부위는 기억하지 못함)에 발생한 비수포성의 바늘로 쿡쿡 쑤시는 듯한 통증으로 로컬 의원에서 대상포진 Dx. po-med함.
-
5) 2017년경 로컬 의원에서 허리 부위의 대상포진 Dx. po-med함.
-
6) 2017년경 건강검진에서 thyroid US상 갑상선 결절 Dx. no-tx.
-
7) 2020년경 건강검진에서 ovary US상 좌측 난소낭종 Dx. no-tx.
-
8) 2021년 5월경 건강검진에서 breast US상 좌측 유방결절 Dx. no-tx.
-
9) 2021년 5월경 혈변 증상으로 빛가람종합병원에서 colonoscopy상 허혈성 결장염 및 과민성 대장염 Dx. Adm-tx. po-med함.
-
10) 2021년 7월경 우측 등과 옆구리의 통증으로 신장결석이 의심되어 광주기독병원 신장내과에서 abd-CT상 N-S Dx. 그러나 환자가 대상포진 과거력을 말하자 그럴 수도 있다고 듣고 항바이러스제 복용함.
-
11) 2021년 8월경 로컬 병원에서 upper abd-US상 간에 물혹이 있다고 들음. no-tx.
-
12) 2021년 8월경 로컬 병원에서 과민성 대장염 Dx. po-med함.
-
-
복용 약물
본 환자는 영암한국병원으로부터 2021년 8월 23일부터 2021년 8월 29일까지 대상포진 증상에 대하여 약물을 처방받아 복용하고 있었다. 처방된 약물로는 항바이러스제(팜시버정 250㎎ 1일 3회), 항히스타민 및 항알러지약 2종(페니라민정 2㎎ 1일 3회, 엘트리진정 5㎎ 1일 1회), 부신피질호르몬제(니소론엠정 1일 3회)가 포함되어 있었다. 그러나 본원에 입원할 때 자택에서 약을 가져오지 않아 복용이 중단되어, 본원 양방내과에 협진을 의뢰하여 주사제와 외용제를 처방받았다.
-
계통적 문진
-
검사 소견
-
1) 입원 당일 활력징후 : 혈압 120/70㎜Hg, 체온 36.3℃, 맥박수 64회/min, 호흡수 20회/min
-
2) Chest X-ray(2021년 8월 24일) : No visible lung parenchymal lesion.
-
3) EKG(2021년 8월 24일) : Normal sinus rhythm. ST changes in anterior leads.
-
4) 임상 병리 검사(2021년 8월 24일) : Glu 126㎎/㎗(74-109), T-cho 224㎎/㎗(≤199), RBC 3.80×106/㎣(4-6.3), Hct 35.6%(36-46), MCH 32.3pg(26-32), PCT 0.147%(0.18-0.36)
-
5) 한방 검사(2021년 8월 24일)
-
-
평가 방법
-
1) 사진 촬영
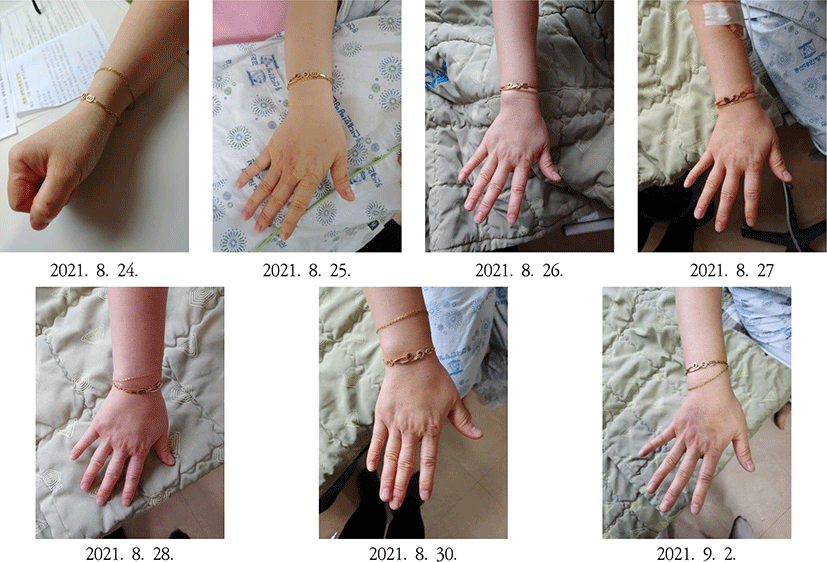
우측 안면부와 오른손에 발생한 대상포진 병변의 변화를 기록하기 위하여 휴대폰 카메라로 환부 사진을 촬영하였다. 입원 당일부터 입원 첫 주 동안은 매일 사진을 촬영하였으며, 2021년 8월 30일부터는 피부 병변이 거의 완치되어 2021년 8월 30일 및 퇴원 당일에 마지막으로 사진을 촬영한 후 촬영을 종결하였다.
-
2) 자각 증상의 평가
대상포진으로 인하여 환자가 자각하는 불편감 및 좌측 안면부와 경부의 소양감을 평가하기 위하여 numerical rating scale(NRS)을 사용하였다. NRS는 환자가 자각하는 불편감 또는 통증에 대하여 전혀 불편하지 않은 경우를 0점, 상상할 수 없을 만큼 가장 불편한 경우를 10점으로 배정하였으며, 환자가 직접 답변하게 하여 평가하였다.
-
-
입원기간 : 2021년 8월 24일 – 2021년 9월 2일
-
치료 방법
-
1) 침 치료
침 치료는 0.25㎜×30㎜ 1회용 멸균 stainless steel 호침(동방침, 동방메디컬, 대한민국)을 사용하여 1일 2회(주말에는 1일 1회) 시행하였다. 2회의 치료 중 1회는 대상포진에 대하여 침 치료를 시행하였으며, 우측 合谷(LI4), 中渚(TE3), 外關(TE5), 地倉(ST4), 頰車(ST6), 下關(ST7), 顴髎(SI18), 迎香(LI20), 水溝(GV26), 承漿(CV24)의 10개 혈위를 취혈하였다. 입원 당일 환자가 평소 있던 요통 증상에 대해서도 치료받기 원하여 침 치료 2회 중 1회는 요통에 대하여 침 치료를 시행하였고, 양측 氣海兪(BL24), 大腸兪(BL25), 關元兪(BL26)를 포함하여 L3-L5 높이에 해당하는 양측 足太陽膀胱經 1선 및 2선상의 阿是穴 10개 혈위를 취혈하였다. 刺鍼 후 별도의 수기법은 시행하지 않았으며, 15분간 留鍼하였다.
유침 시간 동안 전침 자극, 환부 적외선 조사 및 전자뜸 시술을 병행하였다. 전침 시술은 침전기자극기(STN-330, ㈜스트라텍, 대한민국)를 이용하여 시행하였다. 대상포진에 대해서는 우측 合谷(LI4)-外關(TE5), 地倉(ST4)-頰車(ST6)에 1㎐의 빈도로 자극을 주었으며, 요통에 대해서는 양측 氣海兪(BL24)-關元兪(BL26)에 4㎐의 빈도로 자극을 주었다. 자극 강도는 환자가 자극감을 느끼되, 불편감으로 느껴지지 않을 정도의 세기로 설정하였다. 전자뜸(새뜸, ㈜동제메디칼, 대한민국)은 대상포진의 경우 양측 合谷(LI4)에, 요통의 경우 허리 양측 阿是穴 2개 혈위에 45℃의 온도로 시술하였다.
-
2) 약물 치료
-
① 한약
한약은 2첩 당 3팩, 1팩 당 120㏄로 전탕하였고, 1일 3회 식후 30분에 복용하였다. 입원 당일인 2021년 8월 24일에는 平陳健脾湯을 1일분 투여한 다음, 다음날 消風淸營湯으로 처방을 변경하고 1일분을 투여하였다. 2021년 8월 26일부터는 十全大補湯을 加減하여 투여하였으며, 퇴원할 때도 한약을 추가로 처방하여 2021년 9월 8일까지 복용하도록 하였다.
-
② 엑스제
대상포진 또는 요통 개선을 위한 엑스제는 투여하지 않았으나, 2021년 8월 27일 환자가 인후부의 칼칼함을 느껴 약을 복용하기 원하여 2021년 8월 27일부터 증상이 완치된 2021년 8월 30일까지 連翹敗毒散 연조엑스제(한풍제약, 대한민국)를 1일 3회 식후 30분에 투여하였다.
-
-
3) 약침 요법
대상포진 증상에 대하여 紫河車 약침(기린한의원 부설 원외탕전실, 대한민국)을 1일 1회 시술하였다. 30G 0.5㏄ 인슐린 주입용 주사기(FEELject, ㈜필텍바이오, 대한민국)를 이용하여 약침액 0.5㏄를 우측 外關(TE5)과 地倉(ST4)에 동일한 양으로 나누어 시술하였으며, 이외에도 양측 腎兪(BL23), 氣海(CV6)에도 시술하였다.
-
4) 기타 한방 치료
침 치료, 한약, 약침요법 외에도 부항 요법과 물리 치료를 병행하였다. 부항요법은 요통 증상에 대하여 1일 2회 시행하였으며, 양측 足太陽膀胱經 1선과 2선을 포함하는 腰部 阿是穴에 시행하였다. 습부항을 시행하는 경우 양측 腰部 阿是穴 2개 혈위에 시행하였다. 월요일, 수요일, 금요일 주 3일만 건부항과 습부항을 각각 1회씩 시행하였으며, 나머지 요일에는 건부항만 1일 2회 시행하였다.
물리 치료는 일요일을 제외한 주 6일 동안 1일 1회 시행하였다. 요통 증상에 대해서는 온습포 치료, 경피 전기 자극 치료(transcutaneous electrical nerve stimulation), 극초단파 요법(microwave)을 시행하였으며, 오른손 및 얼굴의 대상포진 병변에는 레이저 치료를 시행하였다.
-
5) 양방 치료
본원 양방내과에 협진을 의뢰하여 주사제와 외용제를 처방받았다. 2021년 8월 24일부터 2021년 8월 26일까지는 항히스타민제(휴온스클로르페니라민말레산염주사액, ㈜휴온스, 대한민국) 1앰플을 1일 1회 근육 주사로 투여하였으며, 정맥주사로는 비타민 C(메리트씨 20㎖, ㈜휴온스, 대한민국), acyclovir(클로바주, 명인제약 ㈜, 대한민국), 부신피질호르몬제(프레디솔 125㎎)를 생리식염수와 혼합하여 투여하였다. 비타민 C는 1일 1회 1앰플을 투여하였고, acyclovir는 매회 1앰플씩 1일 3회, 부신피질호르몬제는 매회 1앰플씩 1일 2회 투여하였다. 2021년 8월 27일부터 2021년 8월 28일까지는 acyclovir만 매회 1앰플씩 1일 3회 정맥주사로 투여하였다. 외용제로는 입원 당일에 acyclovir 크림(하원아시클로버크림 5g, ㈜하원제약, 대한민국)이 환자에게 제공되어 대상포진이 발생한 환부에 바르도록 하였다.
-
-
연구 윤리
피부 병변의 경과 관찰 및 기록을 위해 환부 사진을 촬영하기 전에 대상자에게 구두로 사진 촬영의 목적을 설명하고 동의를 구한 다음 촬영하였다. 퇴원 전에는 대상자에게 개인정보, 의무기록 및 지금까지 촬영한 사진의 활용에 대하여 충분히 설명한 다음, 개인정보 이용 동의서에 동의 서명을 받았다.
-
치료 경과
-
1) 대상포진으로 인한 자각 증상의 변화
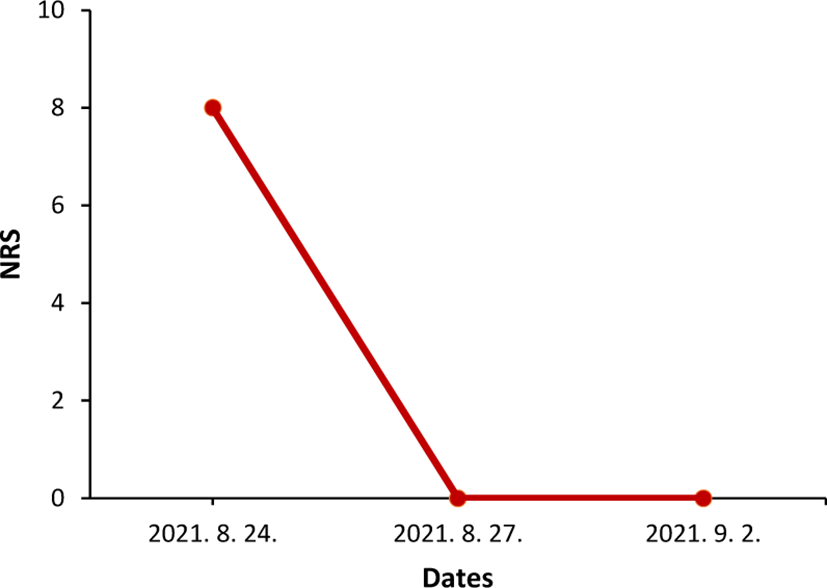
오른손 및 얼굴의 대상포진으로 인해 환자가 자각하는 불편감의 정도는 NRS로 평가하였다. 그 결과, 입원 당일인 2021년 8월 24일에는 NRS 8로 평가되었으나, 치료가 진행됨에 따라 2021년 8월 27일에는 환자가 더이상 불편한 건 없다고 하며 NRS 0으로 평가하였다. 이후 퇴원일인 2021년 9월 2일에도 NRS는 0점을 유지한 상태로 퇴원하였다(Fig. 1).
입원 당일 환자가 호소한 피부 병변의 자각 증상으로는 소양감이 주 증상이었으며, 열감과 통증도 미약하게 있었다. 입원 2일째인 2021년 8월 25일에는 오른손 병변에서 소양감은 물론 미약한 열감과 통증도 모두 소실되었다. 얼굴 병변 또한 전일 대비 부종, 열감 및 통증 모두 경감되었다. 2021년 8월 30일에는 얼굴 병변에서도 소양감 및 부종, 열감, 통증이 모두 소실되었으며, 퇴원할 때까지 오른손 및 우측 안면부의 소양감, 열감, 통증이 악화되지는 않았다.
-
2) 피부 병변의 변화
입원 당일인 2021년 8월 24일에 관찰한 오른손 및 우측 얼굴의 수포는 대부분 이미 潰破되어 瘡面이 미란되어 있었으나, 潰破되지 않은 채 수포성 구진의 형태를 띤 것들도 관찰되었다. 수포로부터 흘러나온 삼출물은 없었다. 입원 2일째인 2021년 8월 25일에는 전일 대비 환부의 발적이 더욱 선명하였다. 그러나 2021년 8월 26일부터는 발적이 감소하여 오른손의 병변에서는 홍반이 완전히 소실되었고, 얼굴 병변도 홍반의 면적이 소량 감소하였다. 2021년 8월 27일에는 우측 口角 일대의 병변도 크게 호전되어 처음에는 하나의 판 형태였던 홍반이 口角과 그 상부에 2개의 반점과 같은 형태로 줄어들었다. 이후로도 오른손 및 얼굴의 수포와 발적은 계속하여 감소하였다. 2021년 8월 28일부터는 오른손 병변의 수포들이 소실되기 시작하였고, 2021년 8월 31일에는 오른손의 병변은 이제 수포가 있었던 자리에 하얀 각질로 된 뚜렷한 경계를 지닌 작은 미란면의 형태로만 관찰되었다. 퇴원하는 2021년 9월 2일에는 마침내 얼굴 병변도 완치되어 우측 口角 일대의 홍반이 소실되었다(Fig. 2, 3).
-
Ⅲ. 고찰 및 결론
본 증례는 과거 대상포진이 발병한 과거력이 있으며 최근 COVID-19 백신 접종 후 대상포진이 오른손 및 우측 얼굴에 재발한 것으로 추정되는 환자 1례를 대상으로, 2021년 8월 24일부터 2021년 9월 2일까지 10일간 본원에 입원하여 침 치료, 한약 복용, 紫河車 약침 시술 등의 한방 치료를 시행함과 동시에 본원 양방내과와의 협진 하에 양방 치료를 병행하였다. 그 결과, 퇴원 당일에는 대상포진으로 인하여 오른손과 우측 얼굴에 발생한 피부 병변이 모두 소실되었고, 해당 병변 부위에 발생하는 소양감과 같은 자각 증상으로 인하여 환자가 느끼는 불편감도 입원 당일에 평가한 NRS 8에서 NRS 0으로 감소하였다. 이외에도 입원 당시 환자가 함께 치료를 받기 원했던 요통 증상도 입원 치료 결과 호전된 상태로 퇴원하였다.
대상포진은 감각신경절에 잠복해 있던 VZV가 재활성화되며 통증, 감각이상, 띠 모양으로 군집한 수포를 일으키는 질환으로, 가슴신경(thoracic nerve)을 가장 흔히 침범하므로 반 이상은 몸통에 발생하고, 20% 정도는 얼굴에 발생하며, 평균 2-3주의 경과를 보인다2). 대상포진은 과거 한의학 문헌들에서 ‘纏腰火丹’ 또는 ‘蛇串瘡’으로 언급되어 왔다. 한의학에서 바라본 病因으로는 情志內傷으로 肝氣가 鬱結되어 肝經에 火가 盛하여 발병하거나, 脾失健運으로 蘊濕하고 化熱되어 脾經에 濕熱이 축적되어서 발병하거나, 혹은 年老體虛, 과로로 인한 毒邪의 感受, 濕熱毒性으로 인하여 氣滯血瘀하여 발병한다고 보았다. 또한 발병 부위 및 발병 연령대에 따라 辨證施治가 구분되어 있는데, 肝經火盛한 경우는 頭面部 및 脇肋部에 발병한 대상포진에 해당하며, 淸肝火, 利濕熱하는 龍膽瀉肝湯에 적절하게 가감하여 사용한다. 脾經濕熱한 경우는 복부와 대퇴부에 발병한 대상포진에 해당하며, 健脾利濕淸熱하는 除濕胃笭湯에 鴨跖草를 加하여 사용한다. 氣滯血瘀한 경우는 노약자에서 발생한 대상포진에 해당하며, 利氣活血, 重鎭止痛하는 逍遙散 加 丹參, 玄胡索, 磁石, 牡蠣, 珍珠母를 사용한다1). 서양의학에서에서는 대상포진으로 인한 통증의 억제, VZV의 확산 억제, 2차 감염이나 포진 후 신경통과 같은 합병증의 예방을 목표로 하며, acyclovir, famciclovir, valacyclovir와 같은 항바이러스제를 투여한다. 최근에는 대상포진 백신도 등장하여 50세 이상의 성인을 대상으로 접종이 권고되고 있는데, 대상포진 및 치료가 어려운 포진 후 신경통의 발생률을 낮추어 주는 것으로 알려져 있다2).
입원 당일인 2021년 8월 24일부터 2021년 8월 25일까지 투여한 平陳健脾湯은 正傳加味二陳湯에 香砂平胃散을 合方한 처방으로, 본원에서는 食滯와 痰飮으로 起因된 胃脘痛, 胸腹痞悶, 噯氣, 嘈雜 등의 증상에 응용한다. 본 증례에서 환자는 입원 당일 문진 시 평소 소화가 잘 안 되고, 배에 가스가 자주 찬다고 호소하여, 주소증을 치료하기 위한 한약을 처방하기 전에 먼저 소화불량 및 脹滿 증상을 경감시킬 목적으로 1일분만 처방하였다. 2021년 8월 25일부터 2021년 8월 26일까지는 消風淸營湯을 투여하였다. 消風淸營湯은 《晴崗醫鑑》에 수재되어 있는 처방으로 血燥皮風으로 발생하는 전신의 소양감, 특히 야간에 발생하는 극심한 소양감에 적용할 수 있다17). 본 증례에서는 입원 당시 환자의 수포는 거의 소실되었고 얼굴의 열감 및 소양감, 오른손의 소양감을 주로 호소하였기 때문에 血燥로 辨證하고 1일분을 투여하였다. 그러나 입원 3일째인 2021년 8월 26일부터 十全大補湯을 투여하였는데, 그 이유는 환자가 과거에도 대상포진이 재발한 바 있고, 양방 치료로 인하여 통증과 소양감은 거의 호전되었으나 환자가 피로감을 크게 호소하였으며, 발병 전부터 기력저하와 식욕부진 증상을 호소하였고, 四診 상 面色蒼白, 舌紅, 齒痕, 脈沈細하여 氣血兩虛로 변증하였다. 따라서 氣血兩虛의 대표적인 처방인 十全大補湯을 加減하여 투여하였고, 그 후 환자 상태가 빠르게 호전되었다.
대상포진에 약침 시술을 할 경우, 대표적으로 봉약침과 黃連解毒湯 약침액이 많이 사용되어 왔다18). 본 증례에서는 대상포진으로 인한 피부 병변 부근의 경혈인 우측 外關(TE5)과 地倉(ST4), 양측 腎兪(BL23), 氣海(CV6)에 紫河車 약침을 시술하였는데, 紫河車 약침은 말초성 안면신경마비 또는 동안신경마비 등과 같은 신경계 질환에 주로 사용되는 약침이다19). 그러나 紫河車 약침은 虛損을 補益하고 氣血과 精을 補하는 효능이 있으므로20), 본 증례처럼 재발성 대상포진이고 병변이 회복기로 접어든 상태라면 實證에 적용할 수 있는 봉약침이나 黃連解毒湯 약침보다는 紫河車 약침이 더 적합하다고 판단하여 선택하였다.
일반적으로 대상포진은 치유되면 재발하지 않으며21), 재발하더라도 그 확률은 0.4-6.4% 정도로 극히 낮은 것으로 보고되어 있다22-25). 성별에 따른 재발률은 남성보다 여성에게서 더 높게 나타나는 것으로 알려져 있으며25), 연령대에 따라서는 나이가 많을수록 대상포진의 초발 확률이 높아지나, 오히려 재발 확률은 나이가 젊을수록 더 높은 것으로 보고되었다24,26). 대상포진의 재발률이 나이가 젊을수록 더 높은 이유로는 이러한 사람들은 유전적인 소인으로 인해 면역계의 VZV의 감염 억제 능력이 저하되어 있어 처음 발생하는 대상포진에는 물론 재발에도 더 취약하여 일찍 이환되기 때문으로 추정하고 있다24). 또한 첫 번째 발생한 대상포진과 동일한 피부 분절에 대상포진이 재발할 확률은 16.3%로 보고되어 있다25).
동일한 환자에게서 대상포진이 재발할 경우, 그 간격은 매우 다양하다. 국내에서는 정 등27)이 최근 10년간 대상포진의 재발률을 조사한 결과에서는 원발과 재발 간 간격이 최소 6개월에서 최대 30년까지(평균 4.7년)인 것으로 나타났으며, 김 등26)의 코호트 연구에서는 첫 발병과 첫 재발과의 간격이 최소 181일에서 최대 3,815일(평균 1,062.9일)까지 관찰되었다. 해외의 경우 Qian 등24)의 코호트 연구에서는 45-54세에서는 평균 1.9년, 55세 이상에서는 평균 2.9년 뒤에 재발한 것으로 보고되었고, Shiraki 등25)이 일본 미야자키 현의 환자들을 대상으로 관찰한 연구에서는 대상포진의 재발에 최소 2개월에서 최대 73년(평균 13.71±10.96년)까지 걸린 것으로 나타났으며, Yawn 등22)의 연구에서는 기준이 되는 발병 시점으로부터 최소 96일에서 최대 10년 뒤에 재발한 것으로 나타났다. 본 증례에서 대상포진이 발병한 연도는 2016년, 2017년 및 본 증례에서 소개하는 2021년 8월 20일까지 총 3회였는데, 발병 간격은 각각 1년과 4년 정도의 간격을 두고 재발하였고, 이는 이전 연구들에서 보고된 재발 간격의 범주에 포함되는 시간이다. 그러나 환자의 병력을 청취하였을 때 이번 재발에 영향을 끼쳤을 만한 가장 강력한 선행 요인은 5일 전 받은 COVID-19 백신 접종이라고 추정된다. 또한 2021년 7월 발생한 대상포진 의심 증상이 만약 정말 대상포진이었다면, 이번 재발은 이전 연구들과 달리 너무나 짧은 기간인 약 1개월 후에 발생한 것이므로 COVID-19 백신 접종이 VZV 재활성화에 기여할 수 있다는 유력한 근거가 된다.
우리나라는 2021년 2월 26일부터 코로나바이러스감염증-19(COVID-19) 백신 접종을 시작하였다. 미국과 영국에서 COVID-19 백신의 긴급 사용 승인을 위한 임상시험을 실시한 결과, RNA를 이용한 백신과 nonreplicating viral vector를 이용한 백신 모두 임상시험 도중에 국소 이상 반응이 흔히 나타났으나, 대부분 경도에서 중등도의 이상 반응이었고, 이마저도 백신 접종 후 수일 이내에 소실된 것으로 보고되었다13-15). 이처럼 COVID-19 백신은 비교적 안전한 것으로 입증되었으나, 백신 접종을 개시한 이후 국내 및 해외에서 꾸준히 이상 반응이 신고되어 왔다. 우리나라의 경우, 백신 접종을 개시한 2021년 2월 26일부터 2021년 9월 18일까지 이루어진 57,185,164건의 예방 접종 후 신고된 이상 반응은 242,656건으로 전체의 0.42%에 해당하였는데, 이 중에서 예방 접종 후 접종 부위의 발적, 통증, 부종, 근육통, 발열, 두통, 오한과 같은 일반 이상 반응이 232,716건으로 95.9%를 차지하였으며, 사망, 아나필락시스 등을 포함하는 중대한 이상 반응은 9,040건으로 4.1%를 차지하였다16).
현재 우리나라에서 접종되고 있는 COVID-19 백신은 아스트라제네카, 화이자, 모더나, 얀센의 4개 社 제품이 공급되고 있으며, 백신 접종 후 흔히 나타날 수 있는 이상 반응으로는 두통, 근육통, 어지러움, 피로감, 발열, 메스꺼움 등이 보고되어 있다. 국내의 한 병원에서 아스트라제네카 社와 화이자 社의 COVID-19 백신을 접종받은 의료 종사자들을 대상으로 이상 반응 모니터링을 시행한 결과, 전신 이상 반응이 보고된 비율은 아스트라제네카 社의 백신이 더 높았다28,29). 가장 흔한 부작용은 피로, 근육통, 두통, 38℃ 이상의 발열 순으로 나타났다28). 질병관리청에서 조사 및 발간하고 있는 자료인 《주간 코로나 19 예방 접종 후 이상 반응》에서도 두통(24.1%), 근육통(23.3%), 어지러움(16.2%)의 3가지 증상이 다빈도 임상 증상으로 현재까지 집계되었으며, 백신 제조사별로 살펴보면 아스트라제네카 및 모더나 社의 백신에서는 근육통, 두통, 어지러움 순으로 다빈도 이상 반응이 나타났으며, 화이자 및 얀센 社 백신에서는 두통, 근육통, 어지러움 순으로 다빈도 이상 반응이 나타났다16).
그러나 COVID-19 백신 접종으로 인한 이상 반응은 상술한 증상들 이외에도 다양하게 나타날 수 있다. 국내에서는 아직 학술논문의 형태로 보고된 바는 없으나, 이미 해외에서는 COVID-19 백신 접종 후 대상포진이 발병한 사례들30-38)이 보고되어 있다(Table 2). 2021년 9월 26일 PubMed(https://pubmed.ncbi.nlm.nih.gov/)에서 “covid 19 vaccine”[All Fields] AND “herpes zoster”[All Fields]로 검색하여 17개의 문헌을 확인하였으며, 이 중에서 letter를 포함한 9건의 증례 보고 및 이에 포함된 증례 31례를 고찰하였다. 그 결과 COVID-19 백신 접종 후 대상포진이 발병한 경우는 대부분 40대 이상에게서 나타났으며, 수두, 대상포진 백신 등 VZV 감염과 관련된 과거력이 없는 경우도 많았다. 발병 시기는 백신 접종 후 1주일 이내에 발병한 경우가 많았으며, 환자가 접종받은 백신의 종류는 화이자 社와 모더나 社 제품이 많았다. 본 증례는 2021년 8월 16일에 화이자 社의 백신을 접종받고 5일째 되는 2021년 8월 20일에 대상포진이 재발하였는데, 이는 이전에 보고된 해외 증례들과 유사한 경과를 보인 것이다.
| No. | Author | Published date | Sex | Age | Location of herpes zoster lesion | P/H | Vaccine type | Passed days from vaccination |
|---|---|---|---|---|---|---|---|---|
| 1 | Aksu et al30) | 2021 May | M | 68 | Rt. mammary region Rt. back (T3-T5 dermatomes) |
• Hypertension • Dysrhythmia • Anxiety |
N/A (2nd shot) | 5 |
| 2 | Bostan et al31) | 2021 Jun | M | 78 | Lt. chest (T3-T4 dermatomes) |
• Coronary artery disease • Cerebrovascular accident • Hypertension • Chronic pulmonary obstructive disease • Radical cystectomy and prostatectomy due to bladder cancer |
Inactivated vaccine | 5 |
| 3 | Arora et al32) | 2021 Jun | M | 60 | Rt. thigh (L2-L3 dermatomes) |
• Type II diabetes mellitus • Hypertension |
Inactivated vaccine | 4 |
| 4 | Lee et al33) | 2021 Jul | M | 77 | Mid-abdomen Rt. flank Rt. mid-back |
• Crohn's Disease • Aspergilloma • Psoriasis |
Moderna (1st dose) | 4 |
| 5 | M | 56 | Rt. chest | • Atopic Eczema | Moderna (1st dose) | 4 | ||
| 6 | F | 54 | Lt. back Lt. shoulder Lt. triceps |
• Thyroidectomy • Hysterectomy, • Cholecystectomy • Wide local excision due to melanoma |
Moderna (1st dose) | 5 | ||
| 7 | M | 65 | Lt. axilla Lt. shoulder Lt. triceps |
• Hypertension • Shingles |
Pfizer (2nd dose) | 38 | ||
| 8 | F | 43 | 1) Bump on Rt. neck 2) Rt. collarbone & Rt. lower jaw |
• Hypertension | Pfizer (2nd dose) | 1) 4 2) 8 |
||
| 9 | F | 69 | Lt. axilla Lt. upper breast |
• Polycythemia vera treated with Jakafi • Hypertension • Dyslipidemia • Osteopenia • Psoriasis • Actinic keratosis • Basal-cell skin cancer • Squamous-cell skin cancer • Vaccinated with Zostavax and Shingrix |
Moderna (1st dose) | 4-7 | ||
| 10 | M | 42 | Scattered blistering | • Chickenpox | Moderna (1st dose) | 21 | ||
| 11 | F | 47 | T1 dermatome | • Vascular issues to extremities | Moderna (1st dose) | 15 | ||
| 12 | F | 39 | Rt. back Rt. flank |
• Hypertension • Diabetes mellitus |
Moderna (1st dose) | 5 | ||
| 13 | M | 74 | Mid-chest Rt. arm |
• Kidney failure • Anemia • Hypertension • Gout • Heart failure • Atrial fibrillation |
Pfizer (2nd dose) | 3 | ||
| 14 | M | 48 | Lt. flank | • Chickenpox | Pfizer (1st dose) | 12 | ||
| 15 | F | 68 | Lt. axilla Lt. triceps Lt. scapula |
• Hypothyroidism • Hypertension • Adrenal fatigue • Chickenpox • Hives from stress • Rubella • Measles |
Moderna (1st dose) | 12 | ||
| 16 | M | 46 | Rt. flank | • None | Pfizer (1st dose) | 9 | ||
| 17 | F | 60 | Rt. forehead along hairline | • Thyroid cancer • Gout |
Moderna (2nd dose) | 26-28 | ||
| 18 | M | 43 | Rt. flank and back | • Chickenpox | Moderna (1st dose) | 3 | ||
| 19 | F | 65 | Around and under Rt. eye | • Shingles 10 years prior to current episode • Vaccinated for shingles in 2015 and 2019 |
Moderna (1st shot) | 11 | ||
| 20 | M | 44 | Lt. eyebrow | • None | Pfizer (1st dose) | 5 | ||
| 21 | F | 37 | Lt. back Lt. abdomen |
• None | Moderna (1st dose) | 4-5 | ||
| 22 | M | 69 | Unilateral Rt. back and Rt. arm | • Hypercholesterolemia • Susceptible to poison ivy • Vaccinated for shingles in July 2020 |
Moderna (1st dose) | 14 | ||
| 23 | F | 72 | Lt. arm Lt. upper back Lt. breast |
• Hypertension • Rt. breast cancer • Often itchy |
Moderna (2nd dose) | 5-6 | ||
| 24 | Chiu et al34) | 2021 Jul | M | 71 | Lt. T8 dermatome | • None | Moderna (1st shot) | 2 |
| 25 | M | 46 | Lt. T11 dermatome | • None | AZ (1st dose) | 2 | ||
| 26 | M | 42 | Rt. T10 dermatome | • None | AZ (1st dose) | 7 | ||
| 27 | Thimmanagari et al35) | 2021 Jul | M | 42 | Lt. forehead Lt. upper eyelid Lt. scalp Tip of the nose |
• Asthma • Chickenpox |
J & J | 7 |
| 28 | M | 49 | Rt. forehead (V1 dermatome) |
• Bipolar disorder • Schizophrenia • Hyperlipidemia |
Moderna (1st dose) | 7 | ||
| 29 | David et al36) | 2021 Aug | F | 41 | Lt. lower back | • Varicella • Migraine |
Moderna | 8 |
| 30 | Eid et al37) | 2021 Sep | M | 79 | Rt. thigh | • Hypertension • Coronary artery disease • Antineutrophilic cytoplasmic antibody-related glomerulonephritis |
mRNA vaccine | 6 |
| 31 | Tessas et al38) | 2021 Oct | M | 44 | Lt. upper back Lateral and inner side of the Lt. arm (C5-C6 dermatomes) |
• Dyslipidemia • Active smoking • Mild varicella |
Pfizer (1st shot) | 7 |
COVID-19 백신 접종 후에 대상포진이 발생하는 이유는 일시적인 림프구감소증으로 인한 것으로 추정하고 있다. 림프구감소증은 COVID-19 환자의 70% 이상에서 발생하는 현상이며, 특히 CD4+ 및 CD8+ 림프구의 감소가 현저하게 나타나는 것으로 보고되어 있다39,40). 그런데 이러한 현상은 화이자 社 백신의 1상/2상 임상시험41)과 아스트라제네카 社 백신의 1상/2상 임상시험42)에서도 동일하게 관찰되었다. 이러한 림프구감소증은 일시적이고 백신을 접종한 지 6-8일이 지나면 정상으로 회복되나43), 대상포진의 재발을 억제하는 방어 기전인 세포 매개성 면역반응에 관여하는 T세포에 일시적인 기능 상실이 발생하므로 VZV가 재활성화될 수 있다44-46). 본 증례에서는 입원 당일인 2021년 8월 24일에 시행한 임상 병리 검사에서 백혈구백분율을 확인한 결과, 과립구 64.8%(40-75), 림프구 29.9%(20-45), 단핵구 5.3%(2-10)로 림프구의 백분율은 정상 범위 이내였다. 이는 환자가 본원에 입원한 시점은 이미 백신을 접종받은 날로부터 9일이 경과하였기 때문에, 림프구의 수가 회복되어 정상 범위 이내로 결과가 나온 것이라고 사료된다.
이상의 본 증례는 국내에서는 처음 학술논문의 형태로 보고되는 COVID-19 백신 접종 후 재발한 대상포진 환자에 대한 증례이다. 2021년 8월 24일 본원에 내원한 대상포진 환자 1례를 대상으로 병력을 청취한 결과, 이미 2차례의 대상포진 과거력이 있었으며, 2021년 8월 16일 화이자 社의 COVID-19 백신을 접종받은 지 5일 뒤인 2021년 8월 20일에 대상포진이 오른손과 우측 얼굴에 재발한 상황이라 COVID-19 백신 접종의 이상 반응으로 재발한 대상포진으로 추정하였다. 이후 본원에 입원하여 2021년 8월 24일부터 2021년 9월 2일까지 본원에서 침 치료, 한약 복용, 紫河車 약침 시술을 비롯한 한방 치료 및 본원 양방내과 협진 하에 주사제와 외용제 투여를 병행하였고, 그 결과 대상포진이 일반적으로 평균 2주 정도의 경과를 보이는 것에 비하여 입원 치료를 받은 10일 동안 빠른 호전을 보여, 한양방 협진 치료가 대상포진에 우수한 효과가 있는 것으로 사료된다. 병행한 양방 치료로 인하여 수포와 소양감은 빠르게 호전되었으나, 환자가 기력저하 및 피로감을 크게 호소하여 이에 대해 한방 치료를 시행하여 증상을 개선시켰다.
비록 국내 학계에서 COVID-19 백신 접종 후 대상포진이 발병하였다는 문헌은 아직 출판되지 않았으나, 해외에서는 이미 유사 증례들에 대하여 보고되어 있어 본 증례는 COVID-19 백신 접종 후 이상 반응으로 대상포진이 재발한 것으로 추정되며, 현재 환자는 관계 당국에 백신 접종 후 이상 반응으로 신고한 상태이다. 우리나라가 전 국민을 대상으로 한 COVID-19 백신 접 종에 속도를 올리고 있는 만큼, 향후 의료기관에 내원하는 백신 접종자들에 대한 지속적인 모니터링을 통해 백신의 임상시험 과정에서 미처 발견하지 못한 이상 반응을 빨리 발견하여 적절한 조치와 백신의 안전성 확보가 이루어져야 할 것으로 사료된다.