Ⅰ. 서 론
알레르기성 비염은 특징적인 알레르기 항원에 대한 IgE매개 면역반응으로 염증이 발생하며, 주 증상은 수양성 비루, 코막힘, 재채기 및 가려움증으로, 이러한 증상 중 하나 또는 여러 가지의 증상이 복합된 질환이다1). 선진국과 마찬가지로 알레르기성 비염은 우리나라의 알레르기 질환 중에서 가장 높은 비율을 차지하고 있고2-4), 유병률 또한 매년 증가하고 있으며, 알레르기성 비염으로 인한 증상은 삶의 질을 저해하며, 국내뿐 아니라 전 세계적으로 사회적, 경제적 부담을 주고 있다5,6).
서양의학에서는 알레르기성 비염의 치료로 회피요법, 약물치료 등을 사용하고 있는데, 이 중 회피요법은 가장 안전한 치료법이지만 만족할 만한 치료결과를 얻기는 역부족이며, 약물 치료 또한 두통, 어지럼증, 진전, 불면증 등의 원치 않는 부작용을 일으킬 수 있다. 알레르기비염의 진단과 치료 가이드라인에 따르면, 면역치료법의 사용에 대한 권고가 증가하고 있으나7), 이 또한 부작용과 위험이 있어 사용에 주의가 필요하다.
최근 서양의학의 치료에 잘 반응하지 않는 알레르기성 비염의 경우 한의학 치료가 증가하는 것이 추세이며, 국내외로 알레르기성 비염에 대한 한약과 침구 치료, 추나 치료8-13)에 관한 연구는 다수 진행되어 많은 논문들이 보고되어 있고, 한약비강외용제를 주요 중재로 한 문헌 고찰14) 등도 보고되고 있다. 그러나 위약, 기존 약물 치료, 무처치, 다른 한약 처방 등을 비교 중재로 하여 국소 양약 및 한약비강외용제 효과 비교에 대한 문헌 고찰은 찾기 힘들다. 그러나 양약 및 한약 국소비강외용제의 치료 효과 비교 및 차후 국소 한약비강외용제 개발을 위해 현재까지의 연구 근황을 파악하고자 본 연구에서 양약과 한약비강분무제와 점비액 등을 중심으로 알레르기성 비염에 관한 무작위배정 비교임상시험연구(Randomized controlled trial)들을 조사, 분석하여 그 효과를 비교하였다.
Ⅱ. 연구 방법
2019년 7월 1일까지 국내외에 발표된 논문들을 대상으로 Pubmed, Cochrane library, EMBASE, CNKI, KMBASE, RISS, NDSL, KISS, 한국전통지식포탈, 전통의학정보포탈(OASIS)을 기반으로 검색하였다. 국외 논문검색어는 (External application OR (nose or intranasal or nasal) OR Nasal Sprays) AND ((Plant Extracts OR (Herbal Medicine or herbal)) AND (allergic rhinitis OR (rhiniti* or rhinopath or rhinosinusit or rhinoconjunctivitis or ozena* or hayfever or hay next fever))로 하였고, CNKI에서는 ‘过敏性鼻炎’, ‘变应性鼻炎’, ‘鼻鼽’, ‘变态性鼻炎’, ‘中药’, ‘草药’, ‘中医药’, ‘外用’, ‘外用制剂’, ‘中药喷剂’, ‘外用药液’, ‘喷剂’, ‘雾化吸入’, ‘滴鼻’을 조합하여 추가로 검색하였다. 국내 논문검색어는 상기 검색어와 ‘알레르기성 비염’, ‘비강 분무’, ‘분무’, ‘외용제’, ‘분무 치료’을 조합하여 사용하였다.
피험자의 성별과 연령, 인종, 유병 기간, 증세의 정도에는 제한을 두지 않고, 알레르기성 비염을 진단받은 환자를 대상으로 수행한 연구로서 다음의 기준에 부합되는 연구를 시행하였다.
-
무작위배정 비교임상시험연구 (Randomized controlled trial)
-
국소 한약비강외용제, 즉 한약비강분무제, 한약분무치료 또는 한약점비액이 시험군 중재인 경우
-
국소 양약비강외용제가 대조군 중재인 경우 한편 연구대상 피험자에 비용종, 천식, 비중격 만곡, 화농성 비염, 급성 비염 등 기타 비질환이 동반된 경우; 비 혹은 부비동 수술을 시행한 경우; 연구에 사용된 약물에 대한 알레르기가 있는 경우; 최소 1주일 전 연구 결과에 영향을 미칠 수 있는 약물 복용; 최근 호르몬 치료나 면역 치료가 시행된 경우; 정신질환; 심혈관계, 뇌혈관계, 간장, 신장, 혈액학적 질환이 있는 경우 등이 포함된 연구는 제외하였다.
두 명의 연구자(JHR, OSH)가 독립적으로 검색한 후 제목, 초록을 통해 본 연구와 상관없는 논문을 배제하였고, 나머지 연구의 전문을 확인하여 본 연구 주제와의 적합성을 검토하였다.
발간된 국가 및 사용된 언어와 상관없이 포함기준에 맞는 연구들을 선택하였으며, 연구 디자인은 무작위배정 비교임상시험연구(RCT)만을 포함하였다. 관찰연구, 동물 실험, 고찰 연구들은 제외하였다. 연구의 중재는 시험군은 국소 한약비강외용제를 적용하고, 대조군은 국소 양약비강외용제를 적용한 연구만을 포함하여 국소한약외용제와 국소양약외용제의 효과를 비교해보고자 하였다. 위약, 무 처치, 다른 한약 처방 혹은 한의학적 중재법을 비교중재로 이용하거나 치료 효과에 영향을 줄 수 있는 기존의 약물 치료 및 한약 치료, 침구치료가 적용된 경우는 제외하였다.
최종 선정된 연구에서 발행연도, 연구 대상자 연령, 표본크기, 연구 대상자 기준, 중재법, 비교중재법, 중재 기간, 평가지표 및 결과, 안전성을 추출하였다. 안전성의 경우, 군에 상관없이 보고된 이상사례를 모두 검토하였다. 본 연구의 결과는 연구 간의 이질성이 높아 통계적인 합성을 할 수 없다고 판단하여 정성적 합성법(Qualitative Synthesis)을 통해 기술적으로 제시하였으며 메타분석(Meta analysis)은 시행하지 않았다.
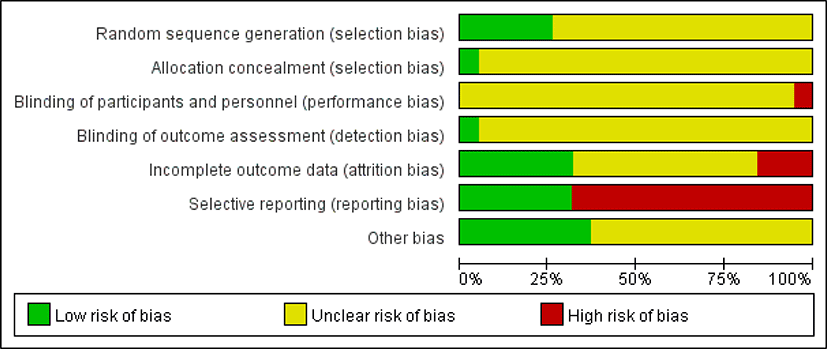
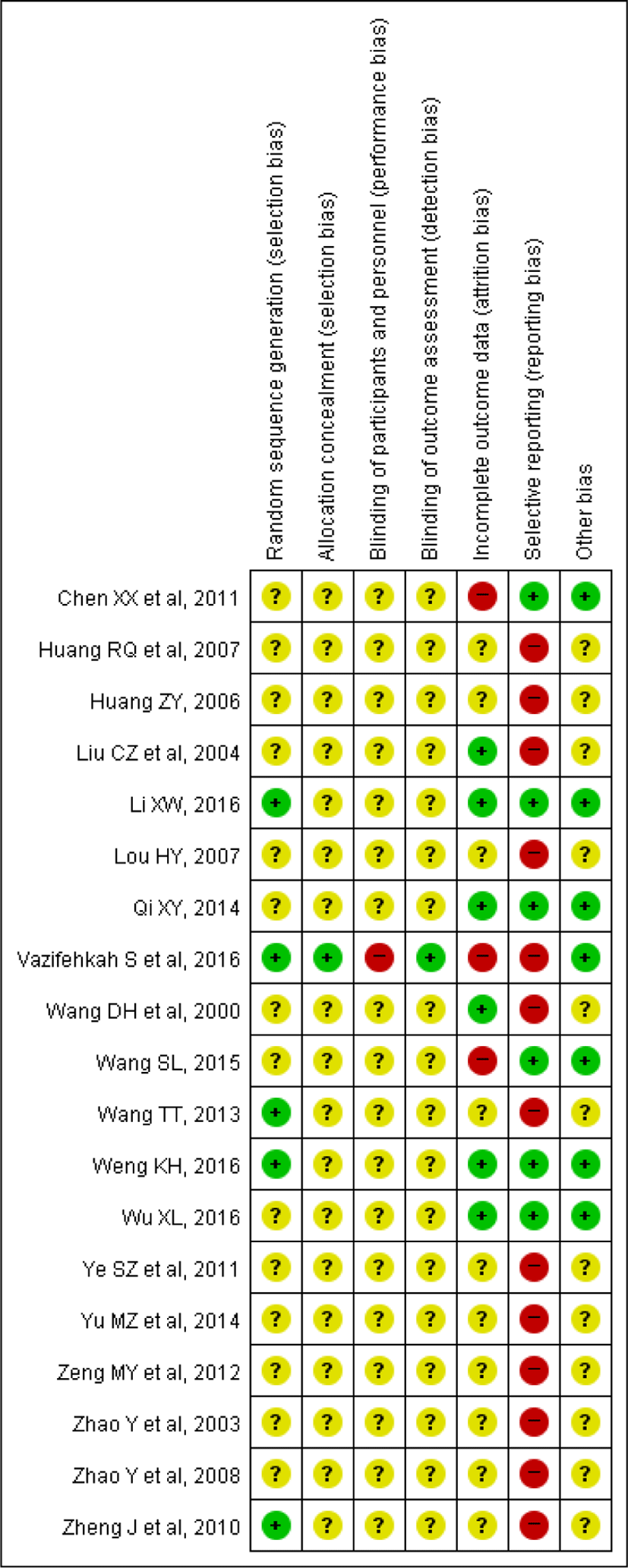
선정된 연구를 대상으로 두 명의 저자가 Cochrane Collaboration의 ‘Risk of bias(RoB) Tool’을 이용하여 독립적으로 질 평가를 시행하였다. RoB Tool은 선택 비뚤림, 실행 비뚤림, 결과 확인 비뚤림, 탈락 비뚤림, 보고 비뚤림의 5가지 비뚤림에 대하여 무작위 배정순서 생성, 배정순서 은폐, 연구 참여자, 연구자에 대한 눈가림, 결과평가에 대한 눈가림, 불충분한 결과자료, 선택적 보고, 다른 잠재적 비뚤림 위험의 일곱 가지 영역으로 구분하여 평가한다. 평가는 각 문항에 대하여 ‘낮음(Low risk)’, ‘높음(High risk)’, ‘불확실(Unclear)’로 구분된다15). 두 연구자의 의견이 일치하지 않는 경우 상호 토론을 통한 합의를 바탕으로 최종 평가를 수행하였다.
Ⅲ. 결 과
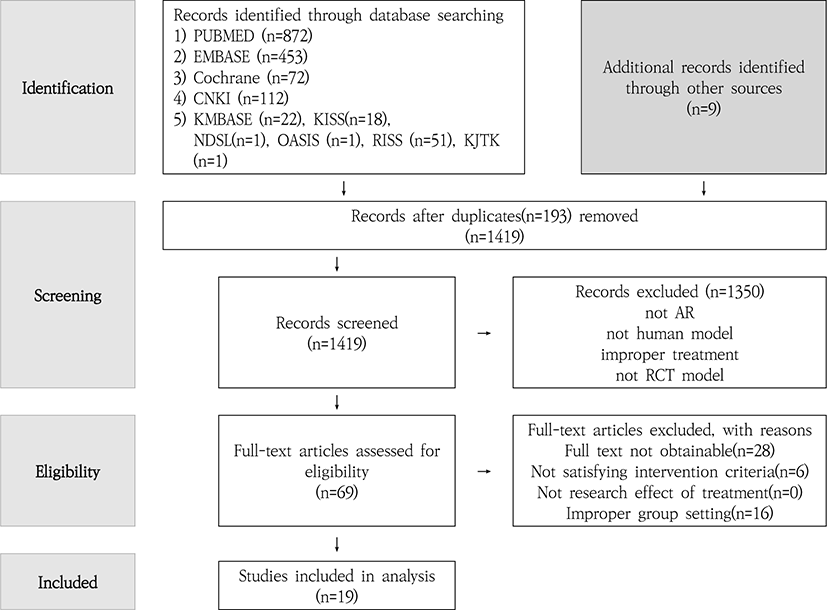
최초 검색 결과 Pubmed 872, EMBASE 453, Cochrane 72, CNKI 112, KMBASE 22, KISS 18, NDSL 1, OASIS 1, RISS 51, 한국전통지식포탈 1편으로 총 1603편의 논문이 검색되었다. 이 외에도 hand searching과 검색한 논문의 참고문헌을 바탕으로 9개의 논문이 추가되어 총 1612편의 논문이 검색되었고, 이 중 중복된 논문 193편을 제외하였다. 제목과 초록을 살펴본 후 69개가 선택되었으며 제외기준에 따라 논문을 제외한 후 최종적으로 19개의 논문이 선정되었다(Fig. 1). 포함된 논문 19편 중 한 편의 논문19)을 제외한 나머지 논문은 모두 중국에서 출판되었다.
연구 대상자 수는 최소 30명에서 최대 400명으로 다양하였다. 한 연구 당 포함된 환자 수는 평균 약 115명이었다. 이 중 전체 연령을 대상으로 한 연구가 11편16-26), 소아청소년을 대상으로 한 연구가 7편28-34)이었으며, 대상자 연령이 언급되지 않은 논문이 1편27)이었다.
알레르기성 비염 진단 기준이 정확히 명시된 제시된 것은 총 19편 중 10편이었다. 중의학적 변증을 시행한 연구는 총 6편이었으며, 이 중 2편18,27)은 氣虛血瘀로 변증한 대상자를 대상으로만 시행하였고, 진단 기준에 중의학적 변증을 더한 연구는 2편28,29), 정확한 변증 기준은 기술되지 않았으나 변증에 따라 중재를 달리 적용한 연구가 2편25,32)이었다.
해당 연구 대상자에 대한 포함기준 및 배제 기준이 모두 명확히 제시된 것은 11편이었다.
주요 중재는 한약점비액을 이용한 연구가 9편, 한약비강분무제가 7편, 초음파분무제가 3편이었다. 중재기간은 3주가 9편으로 가장 많았고, 4주가 6편으로 그 다음으로 많았다. 이 외에 5일, 1주, 2주, 15일이 각 1편씩이었다. 중재의 1일 적용 횟수는 일 2회 적용하는 연구가 9편으로 가장 많았고, 일 1회, 일 3회, 일 4-5회가 각 2편의 연구가 있었다. 이 외 4편의 연구에서는 시험군과 대조군에서 1일 적용 횟수가 달랐다(Table 1).
| Study ID | Participants | Inclusion/Exclusion criteria | Intervention | Treatment period |
|---|---|---|---|---|
| Vanzifehkah S16) (2016) | N = 26, male/female : 15/11, Age range : 23-68 (mean 41.00) | 1) Inclusion criteria i) Patients with presence of chronic rhinosinusitis symptoms for at least 12 weeks ii) Positive CT result indicating the opacity and swelling of the sinus iii) Patients 18 to 75 years of both genders iv) No treatment with systemic or nasal antibiotics or corticosteroids within 4 weeks before visit v) No treatment with oral corticosteroids within the 30 days before visit vi) No treatment with topical corticosteroids within 15 days before visit |
P.anisum-based herbal medicine(Sinupium) 2 drops in each nostril, 2/d (morning, evening), after normal saline irrigation | 4 weeks |
| N = 22, male/female : 14/8, Age range : 18-66 (mean 37.63) | 2) Exclusion criteria i) Nasal and sinus surgery within the last 5 years ii) Moderate to severe asthma and mild asthma that is exacerbated within 30 days before trial iii) Known hypersensitivity to the medication or excipients iv) Acute seasonal allergy v) The signs and symptoms of bacterial sinusitis (fever≥38.5) vi) Other diseases, which in the opinion of the investigator disqualifies the patient for trial enrolment vii) During pregnancy and breastfeeding viii) Any side effect during treatment |
Fluticasone nasal spray 2 puffs (total 200㎍) in each nostril, 2/d(morning, evening), after normal saline irrigation | ||
| Chen XX17) (2011) | N = 57, male/female : 36/21, Age range : 18-53 (mean 27.43) | 1) Inclusion criteria i) Patients had received a diagnosis of PAR - 3 or more symptoms of rhinitis (itching, sneezing, runny nose, and nasal congestion) for at least 30 minutes per day - Physical exam signs : pallor of the nasal mucosa, swollen turbinate - Positive nasal smear of eosinophil, during allergic attack - A positive serum allergens test ii) Patients 16 to 65 year of both genders |
QTNSA 2-3 puffs (0.3ml per puff) in each nostril, 2/d | 2 courses (7days per course) |
| N = 46, male/female : 30/16 , Age range : 17-61 (mean 30.78) | 2) Exclusion criteria i) Acute seasonal allergy, vasomotor rhinitis, sinusitis, nasal polyp ii) During pregnancy and breastfeeding iii) Serious histories of cardiovascular, cerebrovascular, hepatic, renal, hematological and psychiatric diseases iv) Patients refuse treatment methods of this study |
Beconase nasal spray 2-3 puffs (50㎍ per puff) in each nostril, 2/d | ||
| Wang SL18) (2015) | N = 25, male/female : 5/20, Age range : mean 33.76 | 1) Inclusion criteria i) Patients had received a diagnosis of AR ii) With diagnosis of deficiency of Qi and blood stasis, according to TCM iii) Patients 8 to 60 years of both genders iv) No other treatment within 1 week of screening |
Likemin nasal spray, 2 puffs in each nostril, 2/d | 3 weeks of treatment, 4 weeks of follow-up (total 7 weeks) |
| N = 27, male/female : 5/22, Age range : mean 38.55 | 2) Exclusion criteria i) Requiring chronic use of aspirin, glucocorticoid, or corticosteroid; Usage of them within 3 months of screening ii) During pregnancy and breastfeeding iii) Serious histories of cardiovascular, cerebrovascular, hepatic, renal and other diseases iv) Current history of asthma or other atopic disease v) Any clinically significant nasal disease of structural abnormalities(including nasal polyps, septal deviation), chronic sinusitis vi) Severe disease like malignant tumor vii) Receiving immunotherapy (desensitization therapy); Usage of antihistamine within 3 days of screening viii) Participating in other drug clinical trials |
Mometasone furoate nasal spray, 2 puffs in each nostril, 1/d | ||
| Yu MZ19) (2014) | N = 50, male/female : 61/39, Age range : 18-50 | 1) Inclusion criteria i) Patients had received a diagnosis of SAR or PAR that occurs at the same time every year ii) 3 symptoms : swollen turbinate, clear rhinorrhea, sneezing iii) At least a 2-year history of AR iv) Positive nasal smear of eosinophil, during allergic attack |
Fufanggancaosuan nasal drops, 1-2 drops in each nostril, 3/d | 3 weeks |
| N = 50, male/female : 61/39, Age range : 18-50 | 2) Exclusion criteria : Not mentioned | Beclomethasone nasal spray, 1-2puffs in each nostril, 2/d | ||
| Ye SZ20) (2011) | N = 212, male/female : 110/102, Age range : 2-73 | 1) Inclusion criteria i) Patients had received a diagnosis of AR - ≥ 1 year history of AR complained nasal itching, sneezing, nasal obstruction and runny nose - Symptoms of rhinitis for at least 30 minutes per day; at least 6 months per year - Positive skin prick test to a specific allergen - Serum IgE>0.09mg/L |
Ultrasonic nebulization of Cangxinye, 10min, 1/d | 7days per course → total 3 courses |
| N = 188, male/female : 97/91, Age range : 2-73 | 2) Exclusion criteria : Not mentioned | Ultrasonic nebulization of NS 20ml + Gentamycin sulfate 80,000u + Dexamethasone 2mg nebulization, 10min, 1/d, 7days per course → total 3 courses | ||
| Qi XY21) (2014) | N = 38, male/female : 26/12, Age range : mean 31.23 | 1) Inclusion criteria i) Patients had received a diagnosis of AR ii) Patients 18 to 60 years of both genders |
Xinyi nasal drops, 3 drops in each nostril, 3/d | 3 weeks |
| N = 38, male/female : 24/14, Age range : mean 29.28 | 2) Exclusion criteria i) Usage of other steroids/antihistamine within 1 month of screening ii) During pregnancy and breastfeeding iii) Allergic asthma iv) Upper respiratory tract infection vi) Serious histories of cardiovascular, cerebrovascular, hepatic, renal, hematological and other diseases |
Azelastine hydrochloride nasal spray, 1 puff in each nostril, 2/d | ||
| Wang DH22) (2000) | N = 40, male/female : 26/14, Age range : 14-80 (mean 48.00) | Not mentioned | 10% Tuimindibiye 0.1ml nasal drop, 3/d | 15 days |
| N = 30, male/female : 21/9, Age range : 18-75 (mean 44.00) | 1% ephedrine + NS + dexamethasone 0.1ml nasal drop, 3/d | |||
| Zhao Y23) (2003) | N = 80, male/female : 56/24, Age range : 15-45 (mean 31.80) | 1) Inclusion criteria i) Patients who meet allergic rhinitis diagnosis criteria |
Biyanqing nasal drop, 4-6/d, 1/w | 3 weeks |
| N = 42, male/female : 16/26, Age range : 14-45 (mean 31.90) | 2) Exclusion criteria i) Undiagnosed patients ii) Patients who suffer from too many diseases or who have certain other diseases. iii) Patients under 15 or over 45 years iv) During pregnancy and breastfeeding v) Patients who are allergic to this medication vi) Those who may not be able to determine the effectiveness of treatment after taking medicine or may have incomplete clinical data that may affect treatment efficacy or safety judgements. |
Ephedrine Hydrochloride and Nitrofurazone nasal drop, 4-6/d, 1/w | ||
| Huang ZY24) (2006) | N = 71, male/female : 36/35, Age range : mean 49.32 | Not mentioned | Biminshuidibiye 10ml, 2 drops in each nostril, 3/d | 3 weeks |
| N = 65, male/female : 32/33, Age range : mean 48.25 | 1% Furosemide 10ml+Dexamethasone 5mg, 2 drops in each nostril, 3/d | |||
| Huang RQ25) (2007) | N = 85, male/femnale : 75/60, Age range : 10-60 (mean 30.00) | Not mentioned | Fumigation 30ml, 3-5/d, 15mins • Wind-cold pattern • Wind-heat pattern • Lung-heat pattern |
5 days |
| N = 50, male/female : 75/60, Age range : 10-60 (mean 30.00) | Ephedrine 30mg + Dexamethasone 5mg + DW 30ml, ultrasonic nebulization, 2/d, 15mins | |||
| Zhao Y26) (2008) | N = 150, male/female : 90/60, Age range : 14-48 (mean 31.80) | 1) Inclusion criteria : Not mentioned | Biyanqing nasal drop, 4-6/d | 3 weeks |
| N = 105, male/female : 65/45, Age range : 13-49 (mean 31.90) | 2) Exclusion criteria i) Patients who have not received an accurate diagnosis or have other excessive disease ii) Patients under 13 or over 50 years iii) During pregnancy and breastfeeding iv) Patients who are allergic to this medication v) Patients who affect the treatment effect or safety judgement, such as not meeting the criteria, not taking the drug according to the regulations, unable to determine the therapeutic effect, or having incomplete clinical data. |
Furosemide nasal drop, 4-6/d | ||
| Wu XL27) (2016) | N = 21 | 1) Inclusion criteria i) Patients who have been diagnosed with PAR in Western medicine and TCM - 3 or more symptoms of rhinitis (itching, sneezing, runny nose, and nasal congestion) for 30 min-1 hr or more per day, 4 times or more per week. - Physical exam signs : swollen turbinate; pale, gray or light blue or bloody red nasal mucosa; a large amount of watery secretions in the nasal cavity and nasal passages - A positive allergic IgE test - Positive nasal smear for eosinophils during allergic attack - Patients who meet the 'Qi deficiency and blood stasis' pattern ii) Patients with presence of PAR symptoms for at least 1 years iii) Patients 8 to 60 years of both genders iv) No treatment within 4 weeks before visit |
Keminmiaodanbipenwuji nasal drop, 2 drops in each nostril, 2/d (morning, night) | 21 days |
| N = 22 | 2) Exclusion criteria i) Patients who need to take aspirin, glucocorticoids, or long-lasting corticosteroids for a long time or in the last three months ii) During pregnancy and breastfeeding iii) Patients with severe organic disorders in the heart, brain, kidneys, liver, etc. iv) Patients with bronchial asthma or specific dermatitis v) Patients with nasal diseases such as significant septal curvature, nasal polyps or chronic sinusitis vi) Patients with severe illness such as malignant tumor vii) Patients with skin disease or mental illness viii) Patients who are receiving certain immunotherapy or taking antihistamines within 3 days ix) Patients participating in other drug clinical trials |
Mometasone Furoate nasal spray, 2 puffs in each nostril, 2/d (morning, night) | ||
| Weng KH28) (2016) | N = 20, male/female : 11/9, Age range : 3-13 (mean 8.40) | 1) Inclusion criteria i) Patients had received a diagnosis of PAR ii) Patients 2 to 14 year iii) Patients who are suffering allergic attack at first visit iv) Without any treatment (like oral glucosteroids) |
XingBiWenMinNingJiaoJi nasal spray 1 puffs in each nostril, 2/d | 4 weeks |
| N = 20, male/female : 15/5 , Age range : 3-12 (mean 7.00) | 2) Exclusion criteria i) Serious histories of cardiovascular, cerebrovascular, hepatic, renal, hematological and psychiatric diseases ii) During the asthmatic attack iii) Usage of other oral/nasal antihistamine within 1 week of screening or nasal spray/drop steroids within 1 week of screening iv) Usage of systemic steroids within 4 weeks of screening v) Ongoing use of macrolides antibiotics and(or) antifungal drugs |
Budesonide nasal spray, 2/d (total 256㎍ per day) | ||
| Li XW29) (2016) | N = 20, male/female : 14/6, Age range : mean 7.00 | 1) Inclusion criteria i) Patients had received a diagnosis of PAR ii) Patients 3 to 14 year iii) Patients who are suffering allergic attack at first visit |
Xingbiwenmin nasal spray, 1 puffs in each nostril, 2/d(morning, evening) | 4 weeks |
| N = 20, male/female : 15/5, Age range : mean 7.60 | 2) Exclusion criteria i) Usage of other treatment that could affect the deposition of the study medications ii) Serious histories of cardiovascular, cerebrovascular, hepatic, renal, hematological and psychiatric diseases iii) During the asthma attack iv) Any clinically significant nasal disease of structural abnormalities(including nasal polyps, septal deviation, adenoidal hypertrophy), chronic rhinitis(including acute/chronic sinusitis, atrophic rhinitis) v) Known hypersensitivity to the medication or excipients |
Budesonide nasal spray, 1 puff in each nostril, 2/d(morning, evening) | ||
| Zeng MY30) (2012) | N = 100, male/female : 53/47, Age range : 2-14 | 1) Inclusion criteria i) Patients had received a diagnosis of AR - ≥ 1 year history of AR complained nasal itching, sneezing, nasal obstruction and runny nose - Symptoms of rhinitis for at least 30 minutes per day; at least 6 months per year - Positive skin prick test to a specific allergen - Personal or first-degree relative history of allergic diseases - Serum IgE>0.09mg/L |
Ultrasonic nebulization of LXFMB, 10mins, 1/d, 7 days per course → total 3 courses | 7 days per course → total 3 courses |
| N = 100, male/female : 52/48 , Age range : 2-14 | 2) Exclusion criteria : Not mentioned | Ultrasonic nebulization of Gentamicin 80,000U + Dexamethasone(DXM) 2mg, 10mins, 1/d, 7 days per course → total 3 courses | ||
| Luo HY31) (2007) | N = 15, male/female : 9/6, Age range : mean 7.85 | 1) Inclusion criteria i) Patients had received a diagnosis of AR ii) Patients 3 to 14 years of both genders iii) Patients who are suffering allergic attack at first visit |
Xingbiningjiaoji nasal spray, 1 puff in each nostril, 2/d | 4 weeks |
| N = 15, male/female : 9/6, Age range : mean 7.32 | 2) Exclusion criteria i) Usage of other treatment that could affect the deposition of the study medications ii) Serious histories of cardiovascular, cerebrovascular, hepatic, renal, hematological, psychiatric and other diseases |
Budesonide nasal spray, 1 puff in each nostril, 2/d (total 256㎍) | ||
| Liu CZ32) (2004) | N = 140, male/female : 63/77, Age range : 5-16 (mean 12.00) | Not mentioned | Inhalation total 12ml with atomizer, 15min, 2/d • Wind-cold pattern : No.7 6ml+No.1 6ml • Gallbladder heat pattern : No.7 6ml+No.2 6ml • Wind-heat pattern : No.7 6ml+No.6 6ml |
1 week |
| N = 60, male/female : 26/34, Age range : 6-16 (mean 12.00) | Dexamethasone 5mg, Chymotrypsin 5mg, Gentamicin 40,000u, and NS 5ml inhalation, 15min, 2/d | |||
| Wang TT33) (2013) | N = 25, male/female : 15/10, Age range : mean 4.4 | 1) Inclusion criteria i) Patients who meet the criteria for AR diagnosis in Western medicine and TCM ii) Patients 2 to 6 years iii) Patients who are suffering allergic attack at first visit |
Zhongyaodibiye nasal drop, 1-2 drops in each nostril, 2/d (morning, night) | 4 weeks |
| N = 25, male/female : 11/14, Age range : mean 5.2 | 2) Exclusion criteria i) Those who do not meet the diagnostic criteria and inclusion criteria ii) Those who received treatment that could affect the effectiveness indicator of the study |
Sodium cromoglucate nasal drop, 1-2 drops in each nostril, 2/d (morning, night) | ||
| Zheng J34) (2010) | N = 50, male/female : 31/19, Age range : mean 7.68 | 1) Inclusion criteria i) Patients who meet the criteria for AR diagnosis in Western medicine and TCM ii) Patients 3 to 14 years iii) Patients who are suffering allergic attack at first visit |
Zhongyaoxingbiningjiaodiji nasal spray, 1 puff in each nostril, 2/d | 4 weeks |
| N = 50, male/female : 29/21, Age range : mean 7.33 | 2) Exclusion criteria i) Those who do not meet the diagnostic criteria and inclusion criteria ii) Those who received treatment that could affect the effectiveness indicator of the study iii) Poor compliance with diagnosis, treatment and follow-up |
Budesonide nasal spray, 1 puff in each nostril, 2/d(total 256 μg per day) |
시험군의 중재에 사용된 약물 구성은 Table 2에서 정리하였다. 단일 약재로 구성된 것은 1편이었고, 복합 약재로 구성된 것은 16편이었으며, 2편에서는 약재 구성이 언급되지 않았다. 사용 약재들의 빈도를 분석하였을 때, 蒼耳子(Xanthii Fructus)가 10회로 가장 많았으며, 辛夷(Magnoliae Flos) 9회, 白芷(Angelicae Dahuricae Radix) 7회, 薄荷(Menthae Herba) 6회 순으로 많았다. 비교 중재에 사용된 약물은 단일 약물이 12편, 복합 약물치료가 7편이 있었으며, Budesonide nasal spray가 4회로 가장 많았고, Momentasone furoate nasal spray가 2회로 그 다음으로 많았다.
| Study ID | Intervention | Ingredients |
|---|---|---|
| Vanzifehkah S16) (2016) | Sinupium nasal drop | Pimpinella anisum seeds |
| Chen XX17) (2011) | Qumin Tongbi Nasal Spraying Agent (QTNSA) | Astragali Radix 30 g, Magnoliae Flos 10 g, Psoraleae Semen 10g,RubiaakaneNakai10g,BupleuriRadix10g,Forsythiae Fructus10g,MumeFructus10g,AsiaRadix5g |
| Wang SL18) (2015) | Chinese medicine nasal spray of Likemin | Not mentioned |
| Yu MZ19) (2014) | Fufanggancaosuan nasal drops | Not mentioned |
| Ye SZ20) (2011) | Ultrasonic nebulization of Chanxinye | Xanthii Fructus, Magnoliae Flos, Angelicae Dahuricae Radix, Menthae Herba, Scutellariae Radix, Astragali Radix, Cnidii Rhizoma, Fritillariae Cirrhosae Bulbus, Glycyrrhizae Radix, Chrysanthemia Flos, Glycine Semen Preparatum |
| Qi XY21) (2014) | Xinyi nasal drops | Xanthii Fructus, Magnoliae Flos, Centipeda minima, Moutan Cortex Radicis, Ginseng Radix, Scutellariae Radix |
| Wang DH22) (2000) | 10% Tuimindibiye nasal drop | Asiasari Radix et Rhizoma 15g, Atractylodis Rhizoma Alba 10g, Xanthii Fructus 15g, Wolfiporia extensa 12g, Polyporus 10g, Spirodelae Herba 12g |
| Zhao Y23) (2003) | Biyanqing nasal drop | Astragali Radix, Asiasari Radix et Rhizoma, Hydrocotyle sibthorpioides Lam, Magnoliae Flos, Xanthii Fructus |
| Huang ZY24) (2006) | Biminshuidibiye nasal drop | Magnoliae Flos、Angelicae Dahuricae Radix、Stemonae Radix, Arctii Semen, Tribuli Fructus, Houttuyniae Herba, Kochiae Fructus, Hydrocotyle sibthorpioides Lam, Schizonepetae Spica, Menthae Herba |
| Huang RQ25) (2007) | TCM fumigation according to TCM patterns | Wind-cold pattern : Menthae Herba, Saposhnikoviae Radix, Angelicae Dahuricae Radix10g, Hydrocotyle sibthorpioides Lam 10g Wind-heat pattern : Menthae Herba, Angelicae Dahuricae Radix10g, Saposhnikoviae Radix 10g, Lonicerae Flos 10g Lung-heat pattern : Scutellariae Radix, Arctii Semen10g, Menthae Herba 10g, Platycodonis Radix10g, Houttuyniae Herba 10g |
| Zhao Y26) (2008) | Biyanqing nasal drop | Astragali Radix, Asiasari Radix et Rhizoma, Hydrocotyle sibthorpioides Lam, Magnoliae Flos, Xanthii Fructus |
| Wu XL27) (2016) | Keminmiaodanbipenwuji nasal drop | Astragali Radix, Atractylodis Rhizoma Alba, Saposhnikoviae Radix, Moutan Cortex Radicis |
| Weng KH28) (2016) | XingBiWenMinNingJiaoJi nasal spray | Vincetoxicum paniculatum, Borneolum Syntheticum, Bezoar Bovis |
| Li XW29) (2016) | Xingbiwenmin nasal spray | Vincetoxicum paniculatum, Borneolum Syntheticum, Bezoar Bovis |
| Zeng MY30) (2012) | Ultrasonic nebulization of LXFMB | Xanthii Fructus 10g, Magnoliae Flos 5g, Angelicae Dahuricae Radix 10g, Scutellaria Baicalensis 10g, Astragalus membranaceus 20g, Mentha Piperascens 5g, Cnidii Rhizoma 5g, Fritillariae Rhizoma 10g, Glycyrrhizae Radix 5g, Chrysanthemum morifolium 10g, Glycine max 10g |
| Luo HY31) (2007) | Xingbiningjiaoji nasal spray | Borneolum Syntheticum, Calculus Bovis Artifactus, Xanthii Fructus, Vincetoxicum paniculatum |
| Liu CZ32) (2004) | TCM inhalation according to TCM patterns | No.1 : Pinelliae Tuber, Asteris Radix et Rhizoma, Angelicae Decursivae Radix, Salviae Miltiorrhizae Radix No.2 : Trichosanthes kirilowii Maxim, Scutellariae Radix, Fritillariae Thunbergii Bulbus, Armeniacae Semen, Angelicae Gigantis Radix No.6 : Lonicerae Flos, Forsythiae Fructus, Mori Folium, Chrysanthemi Flos, Hydrocotyle sibthorpioides Lam. No.7 : Xanthii Fructus, Magnoliae Flos、Angelicae Dahuricae Radix, Menthae Herba, Houttuyniae Herba |
| Wang TT33) (2013) | Zhongyaodibiye nasal drop | Magnoliae Flos, Moutan Cortex Radicis, Paeoniae Radix, Cnidii Rhizoma, Angelicae Dahuricae Radix, Agastachis Herba, Xanthii Fructus |
| Zheng J34) (2010) | Zhongyaoxingbiningjiaodiji nasal spray | Borneolum Syntheticum, Bezoar Bovis, Vincetoxicum paniculatum, Xanthii Fructus |
전체 연구에서 치료 효율만을 평가지표로 삼은 연구는 5편이었고, 나머지 연구에서는 모두 두 개 이상의 평가지표를 설정하였다. Primary outcome measurement로는 증상 점수, 일반 증상에 대한 VAS 점수, 삶의 질, 치료 효율 등이 활용되었다. Secondary outcome measurement로는 Lund-Mackay scoring(LMs)를 기반으로 한 CT 스캔 점수, 비강기도저항를 채택한 연구가 각각 1편16,17)씩이었으며, 비유발검사(Nasal provocation test)와 피부단자시험(Skin prick test) 및 비도말검사(Nasal smear) 상 양성의 유무를 관찰한 연구가 2편24,26)이었다. 또한 혈액 및 소변 검사 상 특정 인자 수치를 비교하였다17,18,21,27-29, 31,32,34). 특정 인자로는 IgE, IgG, IgA, IL-13, IL-14, TSLP, uLTD4, uLTE4 등이 있었다.
| Study ID | Outcome measures | Outcomes | Author's conclusion indicating effectiveness? | Adverse effects |
|---|---|---|---|---|
| Vanzifehkah S16) (2016) | 22-item Sino-Nasal Outcome Test(SNOT-22), CT scans based on Lund-Mackay scoring(LMs) | 1) SNOT-22 : improved after treatment in both groups, significantly better results in the study group (p=0.012) • study group vs control group : 20.80±16.24 vs 10.36±10.30 • Subscale Rhinological factors(blow nose, sneezing, runny nose, postnasal discharge, and thick nasal discharge) : 7.26±4.38 vs 4.09±3.22 (p=0.007) Ear and facial symptoms : 2.61±3.25 vs 1.09±2.13 (p=0.066) Sleep function : 2.19±2.49 vs 1.72±2.64 (p=0.534) Psychological issue : -0.07±5.92 vs -3.18±4.14 (p=0.534) 2) CT scan based on LMs : improved after treatment in both groups (p<0.05), no significant difference between the two groups after treatment (p=0.067) • study group vs control group : 2.22±2.94 vs 0.76±1.39 |
T>C | 1) Study group increased discharge (n=7) nausea (n=3) headache (n=1) 2) Control group nasal dryness (n=3) bloody discharge (n=1) hoarseness (n=1) |
| Chen XX17) (2011) | Symptoms and signs score, Effective rate, IL-4, IL-8, IgE, Nasal airway resistance (NAR) | 1) Effective rate : no statistical significance between the treatment group and the control group (markedly effective rate 61.40% vs 63.04%, total effective rate 87.72% vs 89.13%) 2) Symptoms and signs integrals : improved after treatment in both groups (p<0.01), no significant difference between the two groups after treatment (p>0.05) • Nasal congestion : 2.45±0.76 → 1.06±0.48 vs 2.24±0.83 → 1.21±0.54 • Sneezing : 2.16±0.88 → 1.13±0.81 vs 2.27±0.91 → 1.05±0.96 • Runny nose : 1.82±0.65 → 0.79±0.46 vs 1.90±0.72 → 0.84±0.53 • Itching : 1.74±0.80 → 0.52±0.37 vs 1.68±0.69 → 0.65±0.48 • Sign of nasal cavity : 2.12±0.91 → 1.26±0.60 vs 1.93±0.96 → 1.47±0.72 3) Serum levels of IL-4, IL-8, IgE, and NAR : significantly decreased after treatment in the two groups, showing statistical difference(p<0.01), no statistical difference between the two groups. (p>0.05) • IL-4 : 91.4±3.3 → 49.9±3.2 vs 92.2±1.3 → 46.6±4.5 • IL-8 : 245.55±25.23 → 159.39±54.381 vs 259.17±26.91 → 168.67±68.09 • IgE : 1437.62±284.16 → 1175.58±159.0 vs 1458.74±256.87 → 1218.05±164.27 • NAR : 0.598±0.123 → 0.365±0.083 vs 0.549±0.119 → 0.389±0.081 |
T=C | Not mentioned |
| Wang SL18) (2015) | Urine leukotriene D4(uLTD4) concentration, Symptoms and signs score, Effective rate | 1) uLTD4 : Before treatment, after 3 weeks of treatment, and 4 weeks of follow-up, no statistically significant difference in both groups (p>0.05) 2) Primary symptoms (such as sneezing, nasal itching, stuffy nose, watery secretions, and turbinate swelling) : improved after treatment in both groups. • After 3 weeks of treatment, no significant difference between the two groups. (p<0.05) • After 4 weeks of follow-up, compared to 3 weeks, watery secretions of treatment group, sneezing, nasal itching of control group increased (p=0.005, 0.002, 0.000<0.05) and turbinate swelling of treatment group decreased (p=0.000), the difference is statistically significant 3) Secondary symptoms (such as shortness of breath, sweating, purple tongue, Thin and choppy pulse(Xi Se Mai)) • After 3 weeks of treatment, significantly improved in both groups, except sweating, purple tongue of study group and shortness of breath of control group; no significant difference between the two groups • After 4 weeks of follow-up, no statistically significance between the two groups 4) Total effective rate : After 3 weeks of treatment, significantly better results in the control group than in the study group (p=0.003); After 4 weeks of follow-up, no statistical significance between the study group and the control group (p=0.610) • after 3 weeks of treatment : 80.0% vs 92.5% (p=0.003) • after 4 weeks of follow-up : 88% vs 85% (p=0.610) |
T<C | 1) Treatment group irritation of the throat (n=1) 2) Control group : none |
| Yu MZ19) (2014) | Symptoms and signs score, Effective rate | 1) Total effective rate : no statistical significance between the study group and the control group • study group vs control group (90.00% vs 88.00%) 2) Both treatments can effectively relief symptoms, such as sneezing, runny nose, stuffy nose, nasal itching, significantly improved better results in study groups (all P<0.05) |
T>C | Not mentioned |
| Ye SZ20) (2011) | Effective rate | 1) Effective rate : significantly higher in the study group than in the control group (p<0.01) • study group vs control group : 98% vs 76% |
T>C | Not mentioned |
| Qi XY21) (2014) | Expression levels of CD34+ and EOS, Symptoms score, Effective rate | 1) Expression levels of CD34+ and EOS : significantly decreased after treatment in both groups • CD34+ : significantly lower in the study group than in the control group (p<0.05) - study group : 4.19±2.23 → 2.53±1.81 - control group : 5.98±1.71 → 3.20±1.01 • EOS : no statistical significance between the study group and the control group (p>0.05) - study group : 5.93±1.65 → 3.14±1.23 - control group : 5.55±1.86 → 3.52±1.16 2) Symptom scores : significantly improved symptoms, such as sneezing, runny nose, congestion, nasal itching in both groups (p<0.05). Xinyi nasal drops reduced congestion significantly more than control group(p<0.05) • sneezing : 1.18±0.83 → 0.45±0.55 vs 1.24±0.85 → 0.89±0.61 • runny nose : 1.39±1.05 → 0.74±0.72 vs 1.03±0.68 → 0.63±0.63 • congestion : 1.27±0.81 → 0.16±0.43 vs 1.11±0.86 → 0.79±0.66 • nasal itching : 0.97±0.64 → 0.55±0.5 vs 1.05±0.87 → 0.61±0.59 3) Total effective rate : no significance difference between the study group and the control group (p>0.05) • study group vs control group : 81.58% vs 76.32% |
T=C | 1) Study group nasal burning sensation(n=2), increased discharge (n=1) 2) Control group : Not mentioned |
| Wang DH22) (2000) | Effective rate | 1) Markedly effective rate : significantly higher in the study group than in the control group • study group vs control group : 65% vs 40% (p<0.05) 2) Total effective rate : significantly higher in the study group than in the control group • study group vs control group : 85% vs 63.33% (p<0.01) |
T>C | 1) Study group Nasal pain (n=1) 2) Control group Headache (n=3) |
| Zhao Y23) (2003) | Symptoms and signs score, Effective rate | 1) Effective rate : significantly better results in the study group, except effective rate (p<0.01) • complete cure rate : 20/80 vs 1/42 • markedly effective rate : 34/80 vs 6/42 • effective rate : 20/80 vs 20/42 2) Symptoms and signs score : significantly improved in study group after treatment (including sneezing, runny nose, nasal congestion, turbinate swelling) (p<0.01) |
T>C | No adverse effects |
| Huang ZY24) (2006) | Symptoms and signs score, Positive response of nasal provocation test, Effective rate | 1) Symptoms and signs scores : significantly better result in treatment group than in the control group after treatment (p<0.01) • 11.03±1.30 → 5.02±1.75 vs 11.94±1.36 → 7.24±1.80 2) Positive response of nasal provocation test : significant decreased in both groups after treatment (p<0.01), significantly better results in the study group (p<0.01) • study group vs control group : 67 → 8 vs 62 → 19 3) Effective rate : significantly higher in the study group than in the control group (p<0.05) • study group vs control group : 92% vs 72% |
T>C | Not mentioned |
| Huang RQ25) (2007) | Effective rate | 1) Effective rate : significantly better results in the study group than the control group (p<0.05) • study group vs control group : 89.41% vs 70.00% |
T>C | Not mentioned |
| Zhao Y26) (2008) | Symptoms and signs score, Effective rate, Positive response of Skin prick test(SPT) and Nasal smear | 1) Effective rate : significantly better results in the study group, except effective rate (p<0.01) • complete cure rate : 26.7% vs 2.9% • markedly effective rate : 36.7% vs 14.3% • effective rate : 28.7% vs 47.6% 2) Symptoms and signs score : After treatment, significantly improved in both group. Biyanqing nasal drop reduced sneezing and runny nose significantly more than control group (p<0.01) 3) Positive response of SPT & nasal smear : significantly decreased in study group after treatment (p<0.01) • positive skin prick test : 140 → 33 vs 100 → 100 • positive nasal smear : 150 → 27 vs 105 → 105 |
T>C | No adverse effects |
| Wu XL27) (2016) | Symptoms and signs score, Effective rate, Serum ECP levels | 1) Symptoms and signs score • No significant improvement in both groups after 7 days of treatment (p>0.05) • After 14 days of treatment, nasal itching of control group significantly improved - Nasal itching : 1.40±0.940 vs 0.80±0.768 (p=0.045) • After 21 days of treatment, primary symptoms and signs (such as nasal congestion, nasal itching, watery rhinitis and turbinate swelling) significantly improved in the control group (p=0.025, 0.023, 0.027, 0.016<0.05) - Nasal congestion : 2.10±0.641 → 1.50±0.889 vs 2.10±0.641 → 0.85±0.813 - Nasal itching : 2.20±0.696 → 1.10±0.788 vs 2.15±0.933 → 0.55±0.686 - Watery rhinitis : 1.80±0.696 → 1.20±0.768 vs 1.95±0.887 → 0.65±0.745 - Turbinate swelling : 2.20±0.616 → 1.50±0.688 vs 1.95±0.934 → 0.95±0.605 • No statistical significance in secondary symptoms 2) Total symptoms and signs score • Before & After 7 days of treatment, no significant difference in both groups • After 14 & 21 days of treatment, significantly improved in the control group (p=0.045, 0.001) - After 14 days : 12.80±3.172 → 9.50±3.236 vs 13.16±2.434 → 7.35±3.313 - After 21 days : 12.80±3.172 → 8.25±2.731 vs 13.16±2.434 → 5.20±2.419 3) Effective rate : significantly higher in the control group than in the study group • study group vs control group : 80.95% vs 95.45% (p=0.034) 4) Serum ECP : significantly decreased after treatment in both group; No significant difference between the two groups • 17.61±16.398 → 15.18±13.608 vs 17.01±14.254 → 16.38±14.254 |
T<C | No adverse effects |
| Weng KH28) (2016) | Serum TSLP, IL-13, IgE, Total symptom score(TSS), Visual analog scale(VAS) for general symptom, Allergic rhinitis Quality of Life Questionnaire(ARQLQ) | 1) Serum levels of TSLP, IL-13, and IgE : significantly decreased after treatment in both group(p<0.01), no significant difference between the two groups after treatment (p=0.725, 0.783, 0.856 >0.05) • TSLP : 151.13±12.83 → 143.43±8.28 vs 159.65±24.42 → 141.35±24.94 • IL-13 : 177.00±112.25 → 114.63±67.93 vs 210.31±69.84 → 119.80±50.72 • IgE : 319.83±129.26 → 189.66±89.79 vs 281.69±111.68 → 184.86±79.77 2) TSS, ARQLQ : improved after treatment in both groups (p<0.01), no significant difference between the two groups after treatment • TSS : 16.50±3.687 → 10.23±3.463 vs 18.60±3.76 → 8.30±4.12 • ARQLQ : 2 → 1 vs 3→1 3) VAS : improved after treatment in both groups, significantly better results in the control group (7.55±1.05 → 2.74±0.68 vs 8.14±0.85 → 2.09±0.50, p<0.01) |
T<C | Not mentioned |
| Li XW29) (2016) | Serum levels of FcεRI, IL-4, IgE, Total Symptom Score(TSS), Visual Analog Scale(VAS), Allergic rhinitis Quality of Life Questionnaire(ARQLQ) | 1) Serum levels of FcεRI, IL-4 and IgE : significantly decreased after treatment in both group, no significant difference between the two groups after treatment (p>0.05) • FcεRI : 681.239±77.205 → 463.239±69.244 vs 693.966±82.413 → 410.129±60.841 • IL-4 : 163.793±21.822 → 106.807±16.124 vs 173.092±19.847 → 106.051±19.528 • IgE : 319.828±27.559 → 189.661±19.143 vs 281.693±24.972 → 184.862±17.837 2) TSS : improved after treatment in both groups, no significant difference between the two groups after treatment (p>0.05) • TSS : 16.50±0.786 → 10.23±0.738 vs 18.60±0.841 → 8.30±0.921 3) VAS : improved after treatment in both groups, significantly better results in the control group (p=0.001) • VAS : 7.545±0.224 → 2.741±0.146 vs 8.135±0.191 → 2.085±0.111 4) ARQLQ : no significant difference in the group (p=0.265) |
T<C | Not mentioned |
| Zeng MY30) (2012) | Effective rate | 1) Total effective rate : significantly higher in the study group than in the control group(p<0.05) • study group vs control group : 98% vs 76% |
T>C | Not mentioned |
| Luo HY31) (2007) | Urine leukotriene E4(LTE4), Symptoms and signs score, Effective rate | 1) Urine LTE4: significantly reduced after treatment in both groups (p<0.01), no significance difference between the study group and the control group (p>0.05) • study group : 130.81±64.77 → 83.58±28.54 • control group : 132.51±64.60 → 75.75±27.12 2) Score of symptoms and signs : After 2 weeks treatment, there were no significance difference between the two groups (p>0.05); After 4 weeks treatment, the score of study group was obviously higher than control group (p<0.05) 3) Effective rate : significantly higher than in the study group than in the control group (p<0.05) • study group vs control group : 93.33% vs 73.33% |
T>C | Not mentioned |
| Liu CZ32) (2004) | IgE, IgG, IgA, Eosinophil, Effective rate | 1) IgE and eosinophil : After treatment, significantly improved in the study group; significant difference in study group compared with control group (p<0.01) • IgE : 699. 33±104. 27 → 592. 10±93. 86 vs 728.25±114.09 → 643.53±99.58 • Eosinophil levels : 4.17±1.25 → 1.35± 0.69 vs 4.31±1.40 → 3.05±1.08 2) IgG : significantly increased in both groups after treatment(p<0.05) • 1008.93±168.18 → 1291.78±183.54 vs 1081.53±171.39 → 1379.62±185.72 3) IgA : No significant difference in the study group and control group 4) Effective rate : significantly better results in the study group (p<0.01) • study group vs control group : 97.86% vs 73.33% |
T>C | Unknown group cough (n=unknown) |
| Wang TT33) (2013) | Effective rate | 1) Markedly effective rate : significantly higher in the study group than in the control group (p<0.05) • study group vs control group : 48% vs 28% 2) Effective rate : no statistical significance between the two groups • study group vs control group : 88.00% vs 80.00% |
T=C | Not mentioned |
| Zheng J34) (2010) | Urine Leukotriene E4(LTE4), Effective rate | 1) Urine LTE4 : After 4 weeks of treatment, significantly decreased in both group(p<0.01), no significant difference between the study and control groups • 131.23±63.65 → 83.58±28.54 vs 132.42±64.13 → 75.75±27.12 2) Effective rate : After 2 weeks of treatment, no significant difference between the both groups(p>0.05), After 4 weeks of treatment, significantly higher in the study group than in the control group(p<0.05) • after 2 weeks of treatment : 96% vs 100% • after 4 weeks of treatment : 96% vs 70% |
T>C | Not mentioned |
19개의 연구의 전반적인 질은 낮은 편이었다. 모든 연구가 무작위 배정을 시행하였으나, 무작위 배정순서 생성에서 ‘낮음’으로 평가한 난수표를 이용한 논문 4편28,29,33,34)과 컴퓨터를 이용한 블록무작위배정을 시행한 1편16)의 논문을 제외하고는 무작위 배정순서 방법에 대한 구체적인 언급이 없었다. 배정순서 은폐는 대상자를 참여시키고 분류한 연구자와 치료를 시행한 연구자를 달리하여 연구를 시행한 1편16)의 논문에서만 ‘낮음’이라 평가하였으며, 나머지 연구는 ‘불확실’로 평가하였다. 연구 참여자, 연구자에 대한 눈가림에서는 단일 맹검으로 설계하여 환자에게 시험군과 대조군의 약물을 눈가림하지 않은 1편16)의 논문은 ‘높음’으로 평가하였으며, 이외에는 구체적인 언급이 없어 ‘불확실’로 평가하였다. 결과평가에 대한 눈가림에서 ‘낮음’으로 평가한 1편16)의 연구는 치료자와 다른 평가자들이 CT scan과 증상 및 삶의 질 설문지를 통해 결과를 평가하였으며, 나머지 연구는 해당 결과를 다루지 않아 ‘불확실’이라 평가하였다. 불충분한 결과자료에서는 중도탈락(Withdrawal)이 없다고 언급한 4편21,27,29,32)의 연구는 ‘낮음’으로 평가하였다. Wang 등22)의 연구에서 부작용이 발생한 경우 몇 일간 치료를 중단한 후 다시 치료를 재개하여 모두 결과에 포함하였으며, Weng28)의 연구에서 중도탈락율이 5% 미만이며, 중도탈락 사유가 경과관찰 탈락으로 두 편 모두 ‘낮음’으로 평가하였다. 시험군 중재의 부작용으로 중도탈락자가 발생한 2편16,18) 의 연구와 5% 이상의 탈락율과 탈락이유를 명시하지 않은 Chen 등17)의 연구은 ‘높음’으로 평가하였다. 선택적 보고를 평가하기 위해 포함된 연구의 프로토콜 연구를 시행하였는지 조사하였지만 대부분의 연구가 프로토콜이 없거나 주요 비염 증상 개별 점수과 같은 결과를 평가하는 주요 평가지표들의 언급된 정보가 불충분한 경우 ‘높음’으로 평가하였다. 그 외 비뚤림은 잠재적 비뚤림 위험이 적은 연구는 ‘낮음’, 그 정도를 평가할 근거가 명확치 않은 연구들은 ‘불확실’로 평가하였다(Fig 2, 3).
포함된 연구 중 증상 점수를 평가한 연구에서 대체적으로 국소 한약비강외용제가 양약비강외용제에 비해 증상 호전에 있어 더 나은 효과가 확인되었다. Chen 등17)의 연구에서 두 군 모두 치료 전과 비교하여 비염의 4대 증상(재채기, 코막힘, 수양성 비루, 비강 소양감) 및 비강 징후들이 유의하게 개선되었으나 두 군 간의 유의한 차이가 보이지 않았다. Wang18)의 연구에서는 증상을 주 증상과 부 증상으로 나누어 평가하였으며, 주증상에는 재채기, 비강 소양감, 코막힘, 수양성 비루, 비종창이 포함되며, 부증상은 ‘氣虛血瘀’에 해당하는 증상 즉, 短氣, 自汗, 舌紫暗, 脈細澁을 평가하였다. 주 증상 점수는 3주간의 치료 후에 두 군간의 유의한 차이가 없었으나, 이후 4주간의 향후 관찰 후 한약비강외용제를 사용한 군에서 수양성 비루 증상은 증가하고, 비종창 증상의 유의하게 완화되었으며, 양약비강외용제는 재채기와 비소양감 증상이 유의하게 증가하였다. Wu27)의 연구에서도 Wang18)의 연구와 같이 주 증상과 부 증상으로 나누어 평가하였으며, 주 증상은 총 3주간의 치료 중 2주차에 양약비강외용제의 비소양감 완화가 유의하게 나타났으며, 치료 3주 후 코막힘, 비소양감, 수양성 비루 및 비종창의 네 가지의 증상 모두 대조군에서 유의하게 낮게 보고되었다, 반면 부 증상, 즉 ‘氣虛血瘀’ 변증 증상에서는 두 군 간의 유의한 차이가 없었다. 두 연구28,29)에서 Total symptom score(TSS)을 통해 비염 증상 점수를 평가하였고, 신체 전반적인 증상에 대해서는 VAS로, 삶의 질은 Allergic rhinitis Quality of the Life Questionnaire (ARQLQ)를 이용하여 평가하였다. 그 결과 TSS와 ARQLQ 점수는 양 군에서 모두 치료 전에 비해 치료 후 유의하게 호전되었으나 두 군간의 차이는 없었으며, VAS는 양약비강외용제가 유의하게 더 효과가 있었다.
Vanzifehkah 등16)과 Chen 등17)은 한약비강외용제와 양약비강외용제의 효과 비교를 위해 각각 Lund- Mackay scoring(LMs)를 기반으로 한 CT 스캔 점수와 비강저항속도(Nasal airway resistance; NAR)를 평기지표로 이용하였으며, 치료 전에 비해 두 군에서 모두 유의하게 호전되나 두 군 사이의 차이는 없었다. 검사 상 양성의 유무를 통해 두 군 간의 효과를 평가하기도 하였다. Huang24)은 비유발검사(Nasal provocation test) 상 유무의 대상자 수를 관찰하였으며, 그 결과 한약비강외용제가 양약비강외용제에 비해 유의하게 낮게 나왔다고 보고하였다. 또한 Zhao 등26)의 연구에서 피부단자검사(Skin prick test; SPT)와 비도말검사(Nasal smear)를 시행하였을 때, 치료 후 시험군에서 대조군에 비해 유의하게 감소하였다.
혈액 및 소변 검사 상 특정 인자 수치를 비교한 9개의 연구 대부분에서 두 군 모두 연구 전과 비교하여 수치의 유의한 변화가 있었으나 2편21,32)을 제외하고 한약비강외용제와 양약비강외용제의 수치 변화 사이의 유의한 통계학적 차이는 없었다. Qi21)의 연구에서 CD34+의 발현 수준은 양약비강외용제에 비해 유의하게 감소하였으나 혈중 호산구 수치(EOS)는 유의한 차이가 없었다. Liu 등32)의 연구에서 혈청 내 IgE와 EOS는 국소 한약비강외용제군이 유의하게 증가하였으나, IgG와 IgA는 두 군간의 유의한 차이가 관찰되지 않았다.
AEs를 언급한 연구 8편 중 3편23,26,27)은 양 군에서 특별한 이상사례가 없었으며, 나머지 연구에서도 모두 경도의 이상사례를 보고하였다. Qi21)의 연구에서는 한약비강외용제를 적용한 시험군에서의 비강작열감 2례, 비분비물 증가 1례만 언급되었으며 대조군에서의 구체적인 언급이 없었다. Vanzifehkah 등16)은 시험군에서 비분비물 증가 7례, 오심 3례, 두통 1례, 대조군에서 비강건조감 3례, 비출혈 1례, 쉰 목소리 1례을 보고하였다. Wang18)은 시험군에서 인후부 불편감 1례, 대조군에서는 이상사례가 없다고 보고하였다. Wang 등22)은 시험군에서 비통 1례가 있었으나 치료 중단 2일 후 소실되어 연구에 재참여하였으며, 대조군에서 두통 3례가 있었으며 4일 후에 소실되었다, Liu 등32)은 전체 대상자 중 기침의 이상사례가 발생하였다고 보고하였으나 구체적인 수는 언급되지 않았다.
Ⅳ. 고 찰
알레르기성 비염은 대표적인 제Ⅰ형 알레르기 질환으로 비점막 염증세포에 대한 IgE 매개반응으로 발생하며 주 증상은 수양성 비루, 코막힘, 재채기 및 가려움증으로, 이러한 증상 중 하나 또는 여러 가지의 증상으로 규정되는 복합적인 질환이다1). 알레르기성 비염을 일으키는 주요 원인으로는 꽃가루, 곰팡이, 집먼지 진드기, 애완동물, 해충 등이 있다35). 선진국과 마찬가지로 알레르기성 비염은 우리나라의 알레르기 질환 중에서 가장 높은 비율을 차지하는 질환이며2-4). 2011년에 시행된 국민건강영양조사 보고서에서 알레르기성 비염의 유병률은 19세 이상 성인에서 13.6%, 6세 이상 소아에서 27.2%로36), 성인뿐만 아니라 청소년 및 소아에서도 높은 유병률로 발생한다고 발표했다. 알레르기성 비염은 신체적, 사회적, 정신적인 삶의 질도 감소시키고, 호흡곤란을 동반한 수면장애를 유발시키며, 소아의 경우 항히스타민제의 사용이 학교생활에도 영향을 끼칠 수 있다. 또한, 알레르기 비염이 기관지천식, 상기도합병증, 분비성 중이염으로 악화될 가능성도 있으며, 소아의 성장에 부정적 영향을 끼치며, 가정의 경제적 부담도 증가시킨다37).
알레르기성 비염의 약물 치료에는 corticosteroid 분무제, 항히스타민제, cromolyn sodium, 항콜린제, 류코트리엔 수용체 길항제 등이 있으며 이에 반응하지 않을 경우 면역요법이 고려된다38,39). 그러나 기존의 약물 치료는 두통, 어지럼증, 진전, 불면증 등의 부작용이 있으며 면역요법은 중등도의 환자에게 사용하는 치료법으로 증상 및 삶의 질 개선에 효과적이지만 고비용이라는 단점이 있다39). 이러한 이유로 알레르기성 비염의 치료로 한의학적 치료가 중국, 대만에서는 활발히 이용되고 있으며40,41) 치료의 편리성 측면에서 한약비강분무제, 한약점비액에 대한 개발도 이루어지고 있다17,42-46).
이에 본 연구에서는 양방 및 한방 국소비강외용제의 치료 효과 비교 및 차후 국소 한약비강외용제 개발을 위해 현재까지의 연구 근황을 파악하고자 본 연구에서 양약과 한약 비강분무제와 점비액 등을 중심으로 알레르기성 비염에 관한 무작위배정 비교임상시험연구(Randomized controlled trial)들을 조사, 분석하였다.
본 연구는 19편의 알레르기성 비염에 대한 국소 한약비강외용제와 양약비강외용제를 비교한 RCT를 바탕으로 체계적 문헌고찰을 시행하였으며, 증상 호전에 있어 한약비강외용제가 양약비강외용제와 동일한 효과 혹은 유의미하게 우수한 효과를 보이고 있으며 혈액 및 소변 검사 상 수치 개선에 있어서는 두 치료가 비슷한 효과를 보이고 있음을 확인하였다.
안전성 면에서 살펴보면 각 연구에서 보고된 AEs를 바탕으로 고려할 때 국소 한약비강외용제를 적용하고 난 후 중등도 이상의 이상반응이 발생하지 않아 안전성을 확인할 수 있었다. 하지만 본 연구에 포함된 연구들은 최대 4주간의 치료 중 AEs를 관찰하였으므로 장기간 이용에 대한 안전성의 근거는 부족하였다.
사용된 국소 한약비강외용제의 제형을 살펴보면 한약점비액이 가장 많았고, 한약비강분무제, 초음파분무제 순이었으며, 특히 소아를 대상으로 한 연구28-34) 7편 중 5편이 분무형태를 이용하였다. 사용된 약재 구성이 언급된 17편의 연구에서 蒼耳子(Xanthii Fructus)가 10회로 가장 많이 사용되었다. 蒼耳子은 compound 48/80을 통해 전신성 아나필락시스, 복강 비만세포의 히스타민 분비 그리고 IgE를 이용한 수동피부아나필락시스반응(Passive cutaneous anaphylaxis; PCA) 등을 억제한다고 알려져 있으며47), Kuo 등48)은 인간 사구체간질세포를 이용한 실험에서 세포의 증식을 억제하고 IL-1β 및 TNF-α의 생성도 감소시킨다고 보고하였다. 뒤이어 辛夷(Magnoliae Flos), 白芷(Angelicae Dahuricae Radix), 薄荷(Menthae Herba) 순으로 많았다. 辛夷는 항염증 효과가 있으며49), Kim 등50)의 연구에서는 compound 48/80으로 유도된 모델에서 이개부종반응과 anti-dinitorphenyl IgE로 유도된 수동피부아나필락시스 반응을 억제하며, 복강 비만세포의 히스타민 분비도 억제한다고 보고하였다. 白芷는 알레르기와 천식에 이용되는 기존 약물인 Montelukast보다 총 염증세포수를 유의하게 감소시키고, 기관지폐포액의 IL-4 및 IL-5의 생산을 현저하게 억제하여 항천식효과가 있으며51), 薄荷는 S. aureus, Shigella dysenteriae, E. coli 등의 성장을 억제하고52), 아세틸콜린으로 유도한 혈관수축을 이완시킨다53).
현재 알레르기비염의 증상을 개선하는데 가장 효과적인 약제로 국소용 스테로이드를 선택하고 있으며, 중등증-중증 알레르기비염 치료의 1차 선택 약제로 인정되고 있다54). 비강 내 스테로이드 사용은 코점막과 상피세포 내 호산구, 호염기구, 비만세포 수를 감소시키고 전달물질(mediator) 방출을 차단하며, 호중구의 주화성(chemotaxis)를 억제하여 염증을 경감시켜 비염의 모든 증상을 완화시킨다. 하지만 장시간 사용 시 비중격에 약물 축적되어 궤양이 생기거나 비중격 천공의 발생 등의 위험이 증가하는 것으로 알려져 있다54). 또한 통년성 알레르기비염이 있는 소아 환자에게 비강 내 beclomethasone을 사용하였을 때, 성장 속도가 감소하였다55)는 연구 논문이 발표되기도 하였으며, 최근 개발된 약제(mometasone, fluticasone, ciclesonide 등은 1년간 사용한 경우, 통계적으로 유의한 성장 저하 및 시상하부-뇌하수체축의 이상은 보고된 바가 없으나, 1년 이상 사용 시 전신적 부작용 여부에 대한 근거는 부족한 실정이다56-59). 또한 고령에서 비강 내 스테로이드제 사용과 백내장 발생 사이의 관련성도 보고된 바가 있다60). 본 연구를 통해 알레르기성 비염에 활용되는 국소 한약비강외용제들을 확인할 수 있었으며, 기존 치료와의 비교 및 AEs가 보고된 바를 보았을 때 알레르기성 비염의 치료에 있어 하나의 유효하면서도 안전성을 갖춘 선택지로써 적용을 검토할 가치가 있을 것으로 생각된다.
본 연구의 한계점은 포함된 19편의 연구 간의 이질성이 높아 메타분석을 수행하지 못하였다는 점에 있다. 19편의 연구 중 평가대상이 되는 주요 중재인 국소한약외용제의 종류가 醒鼻凝胶滴鼻剂(China, People’s Hospital Affiliated to Fujian University of Traditional Chinese Medicine, No. Z20110006)을 활용한 3편의 연구28,29,31)와 鼻炎清滴鼻液(黃芪, 细辛, 鹅不食草, 辛夷, 苍耳子로 구성)를 활용한 2편의 연구23,26)를 제외하고는 각기 다른 중재를 이용한 점은 각 중재에 해당하는 약물의 효과와 안전성의 근거가 충분하지 못하다. 또한 증상의 변화를 평가하기 위한 평가지표가 TNSS와 같은 동일한 설문지 등을 이용하지 않았으며, 일부 연구에서는 점수 평가 기준을 언급하지 않았다. 본 연구에 포함된 연구들의 다수가 비뚤림이 모호하거나 높은 연구가 많으며, 대다수가 중국에서 출판되었다는 점은 향후 진행될 알레르기성 비염에 대한 국소 한약비강외용제의 활용에 대한 연구 설계에 참고되어야 한다.
향후 진행되는 연구에서 비뚤림을 줄이기 위해서는 이중눈가림, 위약대조로 연구를 설계하여야 하며61), 활성약과 위약의 외관 차이를 고려한 적절한 위약이 필요할 것으로 생각된다. 또한 유효성 평가를 위해 이중 눈가림 시험기간은 계절 알레르기비염과 연중 알레르기비염 각각 적어도 2주와 4주가 이루어져야 하며61), 증상 평가를 위한 설문지는 유효율보다는 대표적인 TNSS 등을 이용하는 것을 고려해야 하며, 약물에 따라 코에 나타나는 증상 이외에 다른 증상(non-nasal symptom: 눈 주위 가려움, 눈물, 눈의 충혈, 입천장가려움)에 대한 점수도 고려해야 할 것이다. 뿐만 아니라 계절 알레르기 비염을 대상으로 하는 경우, 시험기간 동안 연구 대상자들의 알레르기 유발 물질 노출 기록도 필요할 것으로 생각된다. 이와 같은 점들을 보완하여 양질의 무작위배정 비교임상시험연구가 시행되어야 하며, 이를 통해 알레르기성 비염에 대한 국소 한약비강외용제의 유효성과 안전성의 근거를 가져야할 것이다.