Ⅰ. 서 론
發頤는 턱 부위, 즉 이하선 부위에 발생하는 연조직염으로 현대 의학의 급성 화농성 이하선염(acute purulent parotitis)에 해당한다. 이는 주로 熱病 후나 수술 후 津液이 손상되어 氣血이 부족하고 이하선의 분비 기능이 저하된 상태에서 毒邪가 침입하거나, 癰疽에 의해 속발성으로 발생한다. 주증상으로는 편측 턱 부위의 통증, 긴장감, 腫脹 및 개구장애가 나타나며, 국소 화농과 함께 오한, 발열 등의 전신 증상을 동반할 수 있다1). 이러한 임상 양상은 유행성 이하선염인 痄腮와 유사하나 전염성 및 화농 유무에서 차이가 있으며, 만성 화농성 이하선염의 급성 발작 시에도 이와 유사한 병리적 소견을 보인다1,2).
《傷寒全生集》에 수록된 連翹敗毒散(이하 YGPDS)은 連翹, 黃芩, 梔子, 玄參, 柴胡, 桔梗, 羌活, 升麻, 川芎, 防風, 薄荷, 牛蒡子, 當歸, 芍藥, 紅花로 구성되어 있다. 본 처방은 熱毒壅結과 氣血瘀滯에 의한 국소 癰瘡證의 紅腫熱痛 및 風熱邪毒이 頭面으로 上攻하여 발생한 發頤 등을 치료하는 데 주로 사용된다3).
기존에 발표된 連翹敗毒散 관련 연구들은 대부분 《東醫寶鑑》의 처방 구성을 따르고 있으며, 상기도 감염4), 알레르기5), 박탈성 피부염6), 丹毒7) 치료 및 항동맥경화, 항염증 효과8) 등에 관하여 연구되어왔다. 《東醫寶鑑》의 連翹敗毒散은 荊防敗毒散에 金銀花와 連翹를 가미한 것으로, 주로 외부 감염에 의한 表證 치료와 항염증 작용에 초점을 맞추고 있다5).
반면, 본 연구에서 주목한 《傷寒全生集》의 YGPDS는 《東醫寶鑑》 처방과 달리 獨活, 前胡, 荊芥 등이 제외되고, 淸熱解毒하는 梔子, 黃芩, 玄參과 活血散瘀하는 當歸, 芍藥, 紅花가 추가된 것이 특징이다9). 이러한 구성은 淸熱藥의 항염증 작용과 活血藥의 散瘀 효과를 통해 頭顏面部 조직의 화농과 부종을 동반한 강력한 염증성 질환인 癰疽와 發頤의 치료에 기여했을 것으로 사료되나, 이에 대한 실험적 연구는 전무한 실정이다.
염증 반응은 조직 손상이나 감염에 대한 방어 기전으로10), 대식세포는 LPS(Lipopolysaccharide)와 같은 자극원에 의해 활성화되어 NO(Nitric Oxide), PGE2 등의 염증 매개 물질과 TNF-α, IL-6, IL-1β와 같은 전염증성 사이토카인(pro-inflammatory cytokines)을 분비한다. 이러한 과정은 주로 NF-κB 및 MAPK 신호 전달 경로의 활성화를 통해 조절되며, MCP-1과 같은 케모카인의 발현을 유도하여 염증을 증폭시킨다11-3).
이에 저자는 《傷寒全生集》의 YGPDS가 염증성 질환에 유의한 효과가 있을 것이라는 가설을 세우고, LPS로 유도된 RAW 264.7 대식세포 모델을 이용하여 염증 매개 물질의 억제 효과와 NF-κB 및 MAPK 기전을 규명하고자 하였다. 아울러 Carrageenan (CA)으로 유도된 족부종(Paw edema) Rat 모델을 통해 YGPDS의 생체 내(in vivo) 항염증 효능 및 안전성을 평가하여 유의한 결과를 얻었기에 이를 보고하는 바이다.
Ⅱ. 재료 및 방법
본 실험에 사용된 連翹敗毒散은 《傷寒全生集》의 처방 구성을 따랐으며3), 구성 약재인 連翹, 黃芩, 梔子, 玄參, 柴胡, 桔梗, 羌活, 升麻, 川芎, 防風, 薄荷, 牛蒡子, 當歸, 芍藥, 紅花는 대원약업사(Daegu, Korea)에서 규격품을 구입하여 정선 후 사용하였다. 1첩 분량인 116 g에 증류수 1.7 ℓ를 가하여 3시간 동안 가열 추출하였다. 추출액은 거즈로 1차 여과한 후, 3,000 ×g에서 3분간 원심분리 하였다. 상층액을 회수하여 0.2 ㎛ 여과지(Nalgene, New York, USA)로 2차 여과한 뒤 Rotary evaporator(EYELA, Tokyo, Japan)를 사용하여 감압 농축하였다. 농축액은 초저온 냉동기(Operon, Gimpo, Korea)에서 24시간 이상 동결 후 동결건조기(LABCONCO, Kansas, MO, USA)를 이용하여 건조분말 20.08 g을 얻었으며, 수율은 17.3%였다. 건조된 시료(YGPDS)는 -20℃에 보관하며 실험 시 DMEM 또는 Saline에 용해하여 사용하였다(Table 1).
세포 배양을 위한 DMEM(Dulbecco's modified Eagle's medium), FBS(Fetal bovine serum), penicillin, streptomycin은 Gibco/BRL(Eggenstein, Germany)에서 구입하였다. 세포 독성 및 NO 측정을 위한 MTT, LPS(Escherichia coli 055:B5)는 Sigma-Aldrich(St. Louis, MO, USA) 제품을, DMSO는 Junsei Chemical(Tokyo, Japan) 제품을 사용하였다. NO 측정에 사용된 Griess reagent system은 Promega(Madison, WI, USA)에서 구입하였다.
Western blot을 위한 1차 항체 중 iNOS는 BD Bioscience(San Jose, CA, USA), I-κBα는 Santa Cruz Biotechnology(Santa Cruz, CA, USA)에서 구입하였으며, NF-κB, p-I-κBα, MAPKs(p-ERK, p-JNK, p-p38), β-actin, Lamin A/C 및 2차 항체는 Cell Signaling(Danvers, MA, USA) 제품을 사용하였다. NC(nitrocellulose) paper는 Schleicher & Schuell(Dassel, Germany) 제품을 이용하였다. Cytokine 측정을 위한 ELISA Kit 중 TNF-α, IL-1β, IL-6는 Pierce Endogen(Rockford, IL, USA), MCP-1은 Thermo Scientific(Waltham, MA, USA) 제품을 사용하였다.
동물 실험용 Carrageenan(CA)은 Sigma Chemical Co.(St. Louis, USA)에서 구입하였으며, 족부종 측정은 Plethysmometer(LE 7500; LETICA Scientific Instruments, Spain)를 사용하였다.
성분 분석을 위한 UPLC는 Waters ACQUITYTM UPLC system(USA)과 Photodiode array detector (PDA)를 이용하였고, 컬럼은 Waters ACQUITYTM BEH C18 column(1.7 ㎛, 2.1×100 ㎜)을 사용하였으며 데이터 분석은 Empower software를 활용하였다. 추출에는 Ultrasonic cleaner(8210R-DHT, Branson, USA)를 사용하였다. 이동상 용매인 Acetonitrile과 Methanol은 각각 JT Baker (Phillipsburg, NJ, USA)와 Junsei Chemical (Tokyo, Japan)에서 구입하였으며, 분석용 증류수는 실험실에서 제조하여 사용하였다. 표준품 중 Forsythoside B, Harpagoside, Arctigenin, Geniposide, Paeoniflorin, Ligustrazine Hydrochloride, α-Pinene은 ChemFaces(Wuhan, China)에서, Baicalin, Decursin, Ferulic acid, Quercetin은 Sigma-Aldrich(St. Louis, MO, USA)로부터 구입하여 사용하였다.
YGPDS의 지표 성분 분석을 위해 각 구성 약재의 주요 성분인 Forsythoside B(連翹), Harpagoside(玄參), Arctigenin(牛蒡子), Geniposide(梔子), Baicalin (黃芩), Decursin(當歸), Paeoniflorin(芍藥), Ligustrazine Hydrochloride(川芎), α-Pinene(薄荷), Ferulic acid(升麻), Quercetin(紅花)을 표준품으로 선정하였다. 각 표준품은 Methanol에 용해하여 1 ㎎/㎖의 표준원액을 제조한 후, 단계적으로 희석하여 12.5, 25, 50, 100 ㎍/㎖의 농도로 검량선을 작성하였다(표준곡선의 결정계수 R2≥0.999).
YGPDS 건조 분말 0.2 g을 70% Methanol 10 ㎖에 녹여 2시간 동안 초음파 추출한 뒤 0.22 ㎛ 필터로 여과하여 검액으로 하였다. 분석은 Waters ACQUITYTM UPLC system과 ACQUITYTM BEH C18 column(1.7 ㎛, 2.1×100 ㎜)을 이용하였으며, 컬럼 온도는 실온을 유지하였다. 이동상으로는 0.1% Formic acid가 포함된 Acetonitrile과 0.1% Formic acid 수용액을 사용하여 기울기 용리(Gradient elution) 방식으로 분석하였으며, 유속은 0.4 ㎖/min, 주입량은 2 ㎕였다.
검출 파장은 Paeoniflorin(230 ㎚), α-Pinene(245 ㎚), Geniposide(254 ㎚), Baicalin(270 ㎚), Forsythoside B, Harpagoside, Ligustrazine Hydrochloride, Ferulic acid(280 ㎚), Decursin(330 ㎚), Arctigenin(360 ㎚), Quercetin(370 ㎚)으로 각각 설정하였다. 각 성분의 정성 확인은 표준품과 검액의 머무름 시간(Retention time)을 비교하였으며, 정량 분석은 피크 면적(Peak area)을 이용해 작성된 검량선에 대입하여 산출하였다(Table 2).
Mouse macrophage cell line인 RAW 264.7 세포는 한국세포주연구재단(Seoul, Korea)에서 분양받았다. 세포는 10% FBS, 100 U/㎖ penicillin 및 100 ㎍/㎖ streptomycin이 포함된 DMEM 배지를 사용하여 37℃, 5% CO2 조건의 Incubator(Sanyo, Gunma, Japan)에서 배양하였다. 실험에는 계대 배양 20회 미만이며 80-90% Confluency 상태인 세포를 사용하였다.
RAW 264.7 세포를 24-well plate에 5×104 cells/well로 분주하여 배양한 후, YGPDS를 농도별(3, 10, 30, 100, 300 ㎍/㎖)로 단독 처리하거나, LPS(1 ㎍/㎖)와 함께 병용 처리하여 18시간 동안 배양하였다. 이후 배지에 MTT solution(0.1 ㎎/㎖)을 첨가하여 4시간 동안 추가 배양하였다. 배양액을 제거하고 형성된 Formazan crystal을 DMSO로 용해시킨 뒤 Microplate reader(Tecan, Männedorf, Switzerland)를 이용하여 570 ㎚에서 흡광도를 측정하였다. 세포 생존율은 대조군에 대한 백분율로 산출하였다.
RAW 264.7 세포를 6-well plate에 5×105 cells/well로 분주하고 YGPDS(10, 30, 100, 300 ㎍/㎖)를 1시간 동안 전처리한 후, LPS(1 ㎍/㎖)를 처리하여 18시간 배양하였다. 배양 후 상등액 50 ㎕를 취하여 96-well plate에 옮기고, 동량의 Griess 시약(1% sulfanilamide in 5% phosphoric acid, 1% α-naphthylamide)과 혼합하였다. 혼합액을 상온의 암실에서 10분간 반응시킨 후 540 nm에서 흡광도를 측정하였다. 각 실험군의 NO 생성량은 대조군(Control)의 흡광도에 대한 비율(Fold change)로 나타내었다.
RAW 264.7 세포를 6-well plate에 5×105 cell/㎖로 분주하여 배양한 뒤, YGPDS(100, 300 ㎍/㎖)를 1시간 동안 전처리 하였다. 이후 LPS(1 ㎍/㎖)를 가하여 18시간 동안 자극하였다. 배양 상등액을 회수하여 IL-1β, IL-6, TNF-α (Pierce Endogen, USA) 및 MCP-1 (Thermo Scientific, USA)의 함량을 각 ELISA Kit(Pierce Endogen, USA; Thermo Scientific, USA) 제조사의 매뉴얼에 따라 측정하였다. 각 성분의 생성량은 표준품의 농도별 흡광도로 작성한 표준곡선에 대입하여 pg/㎖ 단위로 산출하였다.
RAW 264.7 세포의 전세포 추출액(Whole cell lysate)은 세포를 PBS로 세척 후 수집하여 radioimmunoprecipitation(RIPA) buffer (Thermo Scientific, USA)에 Protease/Phosphatase inhibitor cocktail을 첨가한 용액으로 4℃에서 30분간 용해시킨 뒤, 15,000 ×g로 10분간 원심분리하여 상등액을 취하였다. 핵 분획(Nuclear fraction)은 세포를 Hypotonic buffer(10 mM HEPES, 10 mM KCl, 0.1 mM EDTA, 1 mM DTT, 0.5 mM PMSF, 0.5% NP-40)에 부유시켜 4℃에서 10분간 반응 후 원심분리(16,000 ×g, 5분)하여 세포질을 제거하였고, 침전물에 Hypertonic buffer(20 mM HEPES, 400 mM NaCl, 1 mM EDTA, 10 mM DTT, 1 mM PMSF)를 가해 4℃에서 1시간 동안 추출한 뒤 원심분리(16,000 ×g, 10분)하여 상등액을 얻었다.
족부종 조직은 RIPA buffer를 가한 후 조직 파쇄기(Taco Prep Bead Beater, GeneReach, Taiwan)로 균질화하고, 15,000 ×g에서 10분간 원심분리하여 상등액을 취하였다.
추출된 단백질은 BCA protein assay kit로 정량하였다. 동량(20-30㎍)의 단백질을 SDS-PAGE로 전기영동하여 분리한 후 Nitrocellulose membrane으로 전사(Transfer)하였다. Membrane은 Blocking 후 1차 항체(iNOS, I-κBα, p-I-κBα, NF-κB, MAPKs, β-actin, Lamin A/C)와 반응시키고, HRP가 결합된 2차 항체를 처리하였다. 단백질 밴드는 ECL detection reagent (Amersham Biosciences, USA)로 발색시킨 후 Image analyzing system (UVP, USA)을 이용하여 스캔하였다. 각 단백질의 발현량은 β-actin(전세포) 또는 Lamin A/C(핵분획)를 기준으로 보정하였으며, 대조군 대비 비율(Fold change)로 나타내었다.
실험동물은 5주령의 수컷 Sprague-Dawley(SD) Rat을 Orient Bio(Seongnam, Korea)로부터 구입하였다. 동물은 온도 20-23℃, 습도 60%, 12시간 명암 주기(Light/Dark cycle)가 조절되는 사육 시설(ECRS)에서 1주일간 적응시킨 후 실험에 사용하였다. 사료(Nestle Purina Petcare Korea, Seoul, Korea)와 물은 자유롭게 섭취하도록 하였다. 본 동물실험은 대구한의대학교 동물실험윤리위원회(IACUC)의 승인(승인번호: DHU2023-037)을 받아 수행되었다.
실험군은 아무런 처치를 하지 않은 정상군(Normal), 대조군(Carrageenan, CA군), YGPDS 0.3 g/㎏ + CA군, YGPDS 1.0 g/㎏ + CA군, 양성대조군(Dexamethasone 1 ㎎/㎏ + CA군)으로 나누었으며, 각 군당 5마리씩 배정하였다(Table 3).
| Group | Treatment | |||
|---|---|---|---|---|
| CA | YGPDS 0.3 | YGPDS 1.0 | DEXA | |
| Normal | - | - | - | - |
| CA | + | - | - | - |
| YGPDS 0.3 g/㎏ + CA | + | + | - | - |
| YGPDS 1.0 g/㎏ + CA | + | - | + | - |
| DEXA + CA | + | - | - | + |
YGPDS와 Dexamethasone은 CA 투여 전 4일간 매일 1회 경구 투여하였다. 마지막 약물 투여 1시간 후, Rat의 우측 뒷발바닥에 1% Carrageenan saline 용액 100 ㎕를 피하 주사하여 족부종을 유발하였다. 족부종의 정도는 CA 주사 직전(0시간) 및 주사 후 1, 2, 3, 4시간에 Plethysmometer(LETICA Scientific Instruments, Spain)를 사용하여 측정하였다. 족부종의 정도는 아래의 수식을 이용하여 Normal군 대비 각 실험군의 비율(Fold change)로 나타내었다.
Ⅲ. 결 과
YGPDS의 표준화를 위해 구성 약재의 주요 지표 성분 11종(Forsythoside B, Harpagoside, Arctigenin, Geniposide, Baicalin, Decursin, Paeoniflorin, Ligustrazine Hydrochloride, α-Pinene, Ferulic acid, Quercetin)에 대한 정성 및 정량 분석을 수행하였다(Fig. 1A).
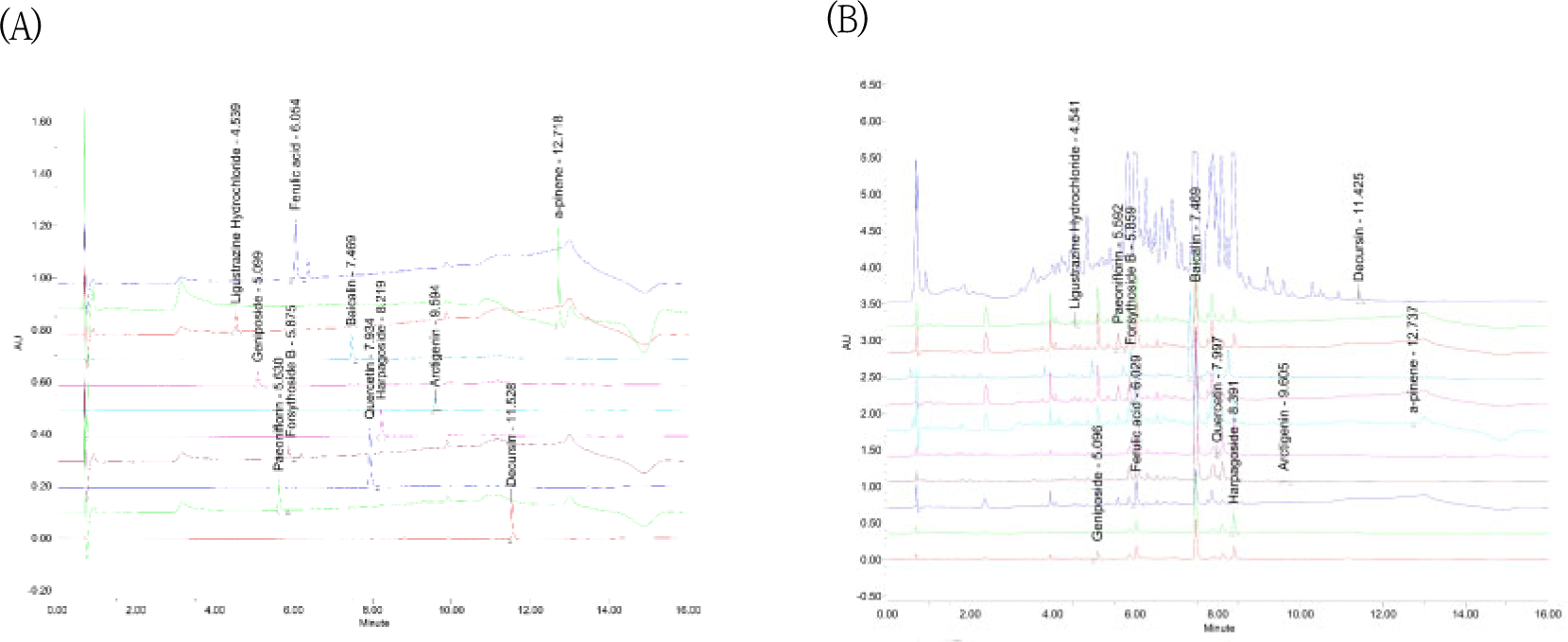
분석 결과, YGPDS 내에는 Baicalin(291.075± 7.719 ㎎/㎏)과 Forsythoside B(143.809±5.714 mg/kg)가 가장 높은 함량으로 존재하였다. 이어 Harpagoside(106.446±4.465 ㎎/㎏)와 Geniposide(102.98±3.581 ㎎/㎏)가 높게 검출되었으며, Ferulic acid(67.851±1.328 ㎎/㎏), Paeoniflorin (45.272±1.233 ㎎/㎏), Ligustrazine Hydrochloride (27.241±2.414 ㎎/㎏), α-Pinene(12.718±1.353 ㎎/㎏, Arctigenin(7.676±0.237 ㎎/㎏), Quercetin (4.477±0.471 ㎎/㎏), Decursin(3.49±0.415 ㎎/㎏) 순으로 함유되어 있음을 확인하였다(Table 4, Fig. 1B).
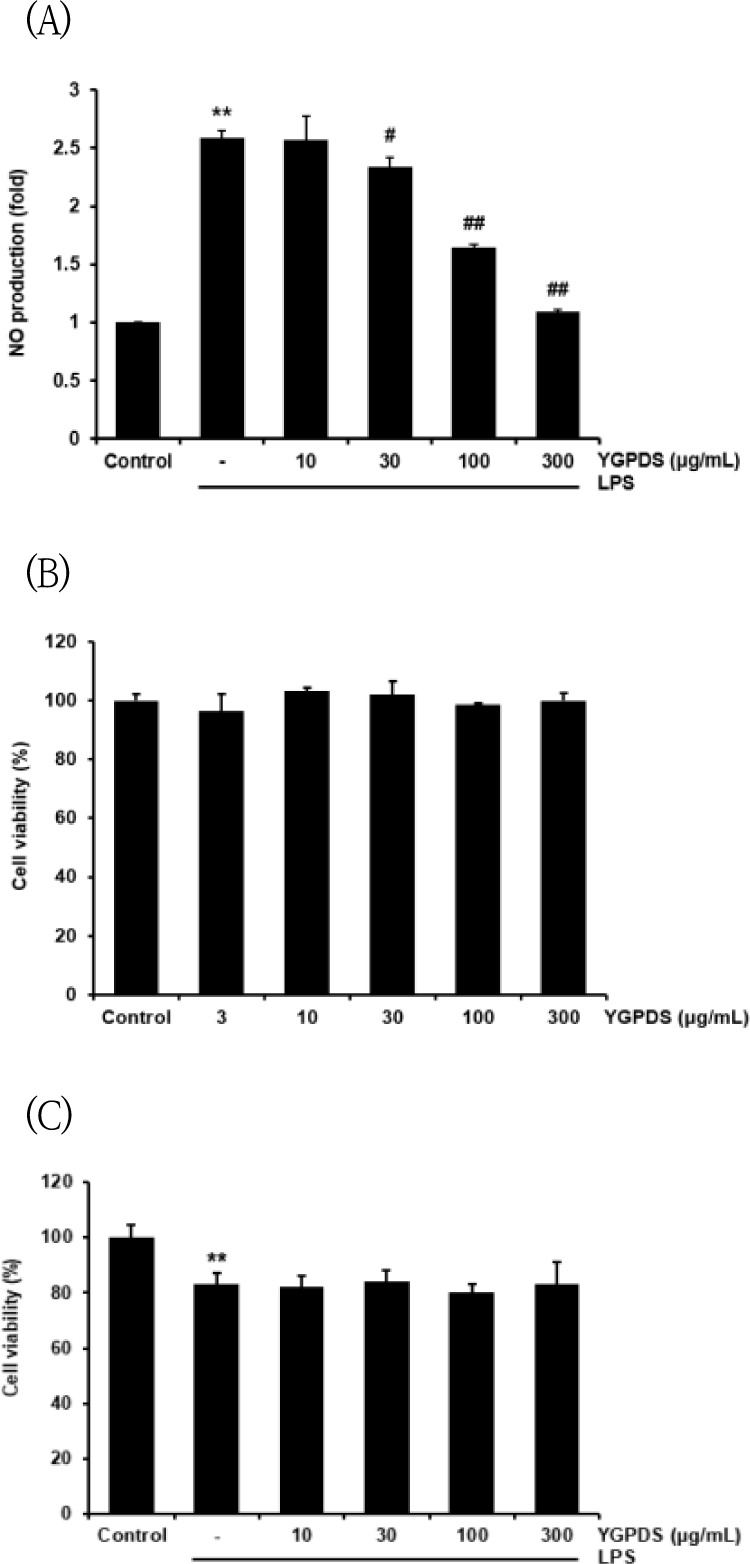
RAW 264.7 세포에 LPS(1 ㎍/㎖)를 단독 처리했을 때 NO 생성량은 대조군 대비 2.59 ± 0.06배로 유의하게 (p<0.01) 증가하였다. YGPDS를 전처리한 결과, 10 ㎍/㎖ 농도(2.58 ± 0.20배)에서는 유의한 억제 효과가 없었으나, 30 ㎍/㎖에서는 2.34 ± 0.08배로 감소하는 경향을 보였다. 특히 100 ㎍/㎖와 300 ㎍/㎖ 농도에서는 각각1.65 ± 0.02배와 1.09 ± 0.01배로 나타나, LPS 단독 처리군 대비 유의하게 NO 생성을 억제하였다(p<0.01) (Figure 2A).이러한 NO 생성 억제 효과가 세포 독성에 기인한 것인지 확인하기 위해 MTT assay를 수행하였다. 먼저 YGPDS의 단독 독성을 평가한 결과, 3, 10, 30, 100, 300 ㎍/㎖ 농도에서 각각 96.46 ± 5.91%, 103.26 ± 1.23%, 101.96 ± 4.62%, 98.59 ± 0.60%, 99.94 ± 2.55%의 생존율을 보여 세포 독성이 관찰되지 않았다. 또한 LPS와 YGPDS를 병용 처리한 경우에도, LPS 단독 처리군83.12 ± 4.06%)과 비교하여 10~300 ㎍/㎖의 모든 농도에서 80.43 ∼ 84.28% 범위의 생존율을 유지하며 유의한 세포 독성을 나타내지 않았다 (Figure 2B, 2C).따라서 YGPDS는 세포 독성 없이 NO 생성을 억제함을 확인하였으며, 억제 효능이 우수한 100 및 300 ㎍/㎖ 농도를 선정하여 이후의 기전 연구를 진행하였다.
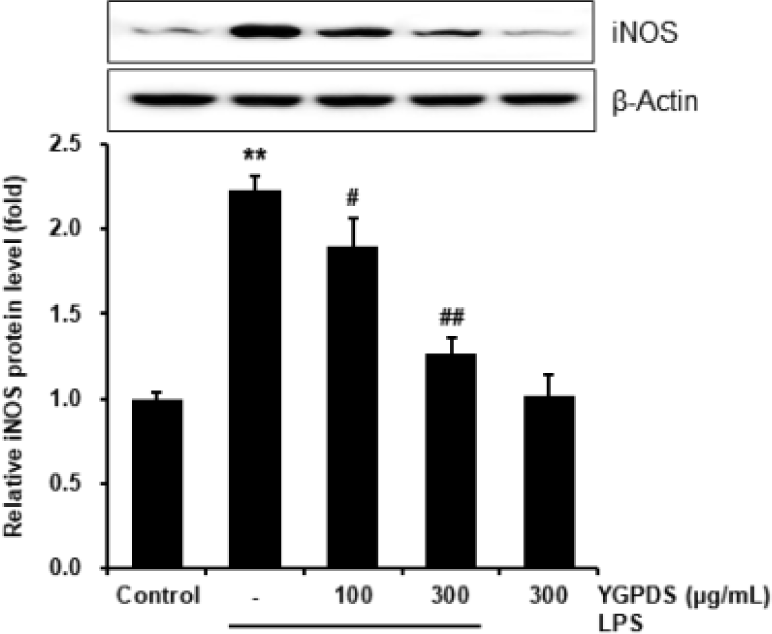
NO 생성의 감소가 합성 효소인 iNOS의 발현 조절에 의한 것인지 규명하기 위해 Western blot 분석을 수행하였다. LPS 자극은 RAW 264.7 세포 내 iNOS 단백질의 발현을 2.23 ± 0.08배로 유의하게 증가시켰다. 그러나 YGPDS를 전처리한 결과, 100 ㎍/㎖ 농도에서는 1.90 ± 0.17배(p<0.05), 300 ㎍/㎖ 농도에서는 1.26 ± 0.09배(p<0.01)로 나타나, LPS에 의해 유도된 iNOS의 발현을 농도 의존적으로 유의하게 억제하였다(Fig. 3). 이는 YGPDS가 iNOS의 단백질 발현을 억제함으로써 NO 생성을 감소시킨다는 것을 시사한다.
YGPDS가 대식세포의 염증 반응 시 분비되는 주요 전염증성 사이토카인(Pro-inflammatory cytokines)의 생성에 미치는 영향을 ELISA로 분석하였다.
먼저 TNF-α의 경우, 대조군(119.22 ± 46.62 pg/㎖)에 비해 LPS 처리군에서 3375.67 ± 76.50 pg/㎖로 유의하게 증가하였다(p<0.01). 그러나 YGPDS를 전처리한 결과, 100 ㎍/㎖ 농도에서 1248.33 ± 66.31 pg/㎖, 300 ㎍/㎖ 농도에서 1021.22 ± 117.57 pg/㎖로 나타나 두 농도 모두에서 LPS 대비 유의하게 감소하였다(p<0.01) (Fig. 4A).
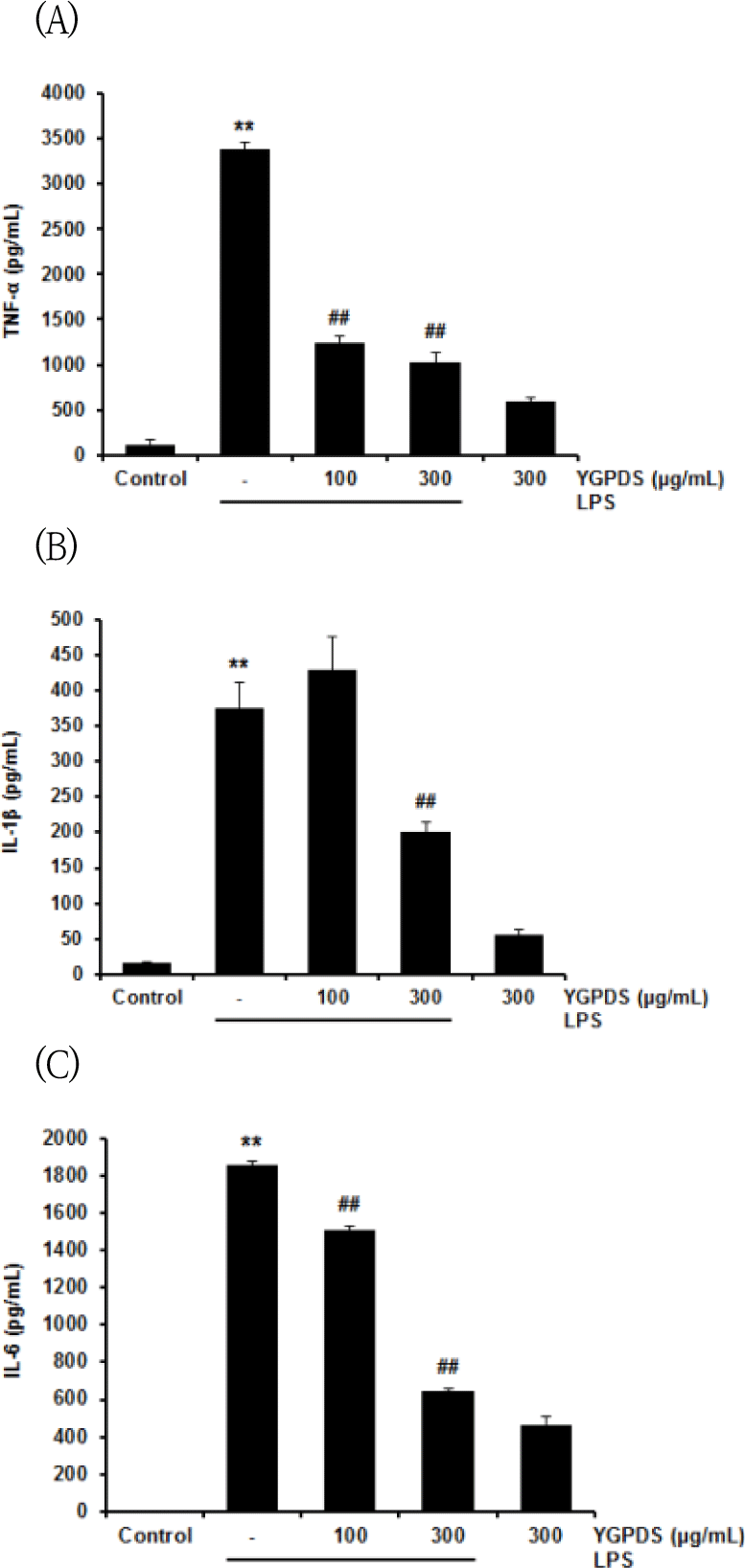
IL-1β 또한 LPS 자극 시 대조군(17.06 ± 0.58 pg/㎖) 대비 374.15 ± 36.82 pg/㎖로 유의하게 증가하였다(p<0.01). 이에 대해 YGPDS 100 ㎍/㎖ 처리군(428.64 ± 46.52 pg/㎖)은 유의한 억제 효과를 보이지 않았으나, 300 ㎍/㎖ 처리군에서는 200.30 ± 14.09 pg/㎖로 생성량을 유의하게 억제하였다p<0.01) (Fig. 4B).
IL-6의 생성량은 대조군(2.39 ± 0.25 pg/㎖) 대비 LPS 처리군에서 1854.17 ± 22.19 pg/㎖로 현저히 증가하였다(p<0.01). YGPDS 전처리는 이를 농도 의존적으로 억제하였으며, 100 ㎍/㎖(1506.25 ± 23.60 pg/㎖)와 300 ㎍/㎖(642.42 ± 18.78 pg/㎖) 농도 모두에서 유의한 감소 효과를 나타내었다(p<0.01)(Fig. 4C).
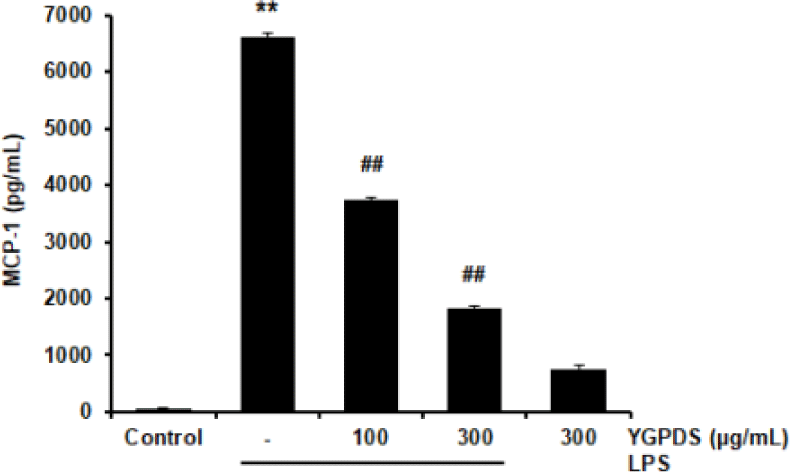
YGPDS가 염증 반응의 주요 매개체인 Chemokine MCP-1의 생성에 미치는 영향을 평가하였다. 정상 대조군(Control)의 MCP-1 생성량은 52.42 ± 10.45 pg/㎖였으나, LPS 단독 처리군에서는 6626.17 ± 59.86 pg/㎖로 대조군 대비 유의하게 증가하였다(p<0.01).반면, YGPDS를 전처리한 군에서는 100 ㎍/㎖ 농도에서 3739.92 ± 34.38 pg/㎖, 300 ㎍/㎖ 농도에서 $1827.83 \pm 50.37$ pg/mL로 나타나, LPS에 의해 유도된 MCP-1의 생성을 농도 의존적으로 유의하게 억제하였다(p<0.01) (Fig. 5).
본 연구에서는 YGPDS가 염증 매개 물질의 발현을 조절하는 주요 전사 인자인 NF-κB 경로를 억제하는지 규명하고자 하였다. 이를 위해 세포질 내 I-κBα 및 p-I-κBα와 핵 분획 내 NF-κB의 단백질 발현량을 Western blot으로 분석하였다.실험 결과, LPS 처리군은 대조군에 비해 세포질 내 I-κBα발현을 0.30 ± 0.09배로 유의하게 감소시켰다(p<0.01). 그러나 YGPDS 전처리군은 100 ㎍/㎖에서 0.51 ± 0.08배(p<0.05), 300 ㎍/㎖에서 0.69 ± 0.08배(p<0.01)로 나타나, LPS에 의한 I-κBα의 분해를 농도 의존적으로 유의하게 억제하였다 (Fig. 6A).
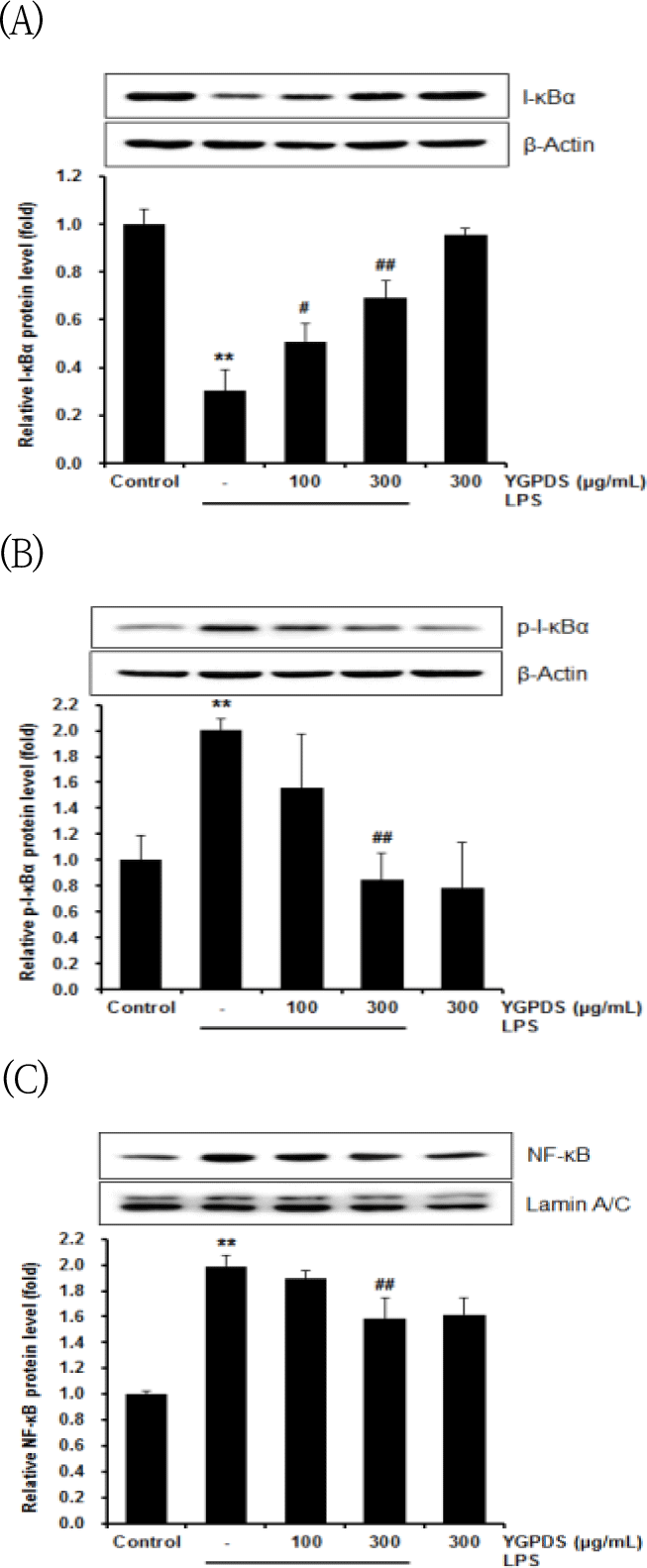
반면, I-κBα의 인산화 형태인 p-I-κBα는 LPS 처리에 의해 2.01 ± 0.09배로 급격히 증가하였으나(p<0.01), YGPDS 300 ㎍/㎖ 처리군에서는 0.85 ± 0.20배로 유의하게 감소하였다(p<0.01) (Fig. 6B).
또한, 핵 내로 이동한 NF-κB(p65)의 발현량 역시 LPS군에서 1.98 ± 0.08배로 증가하였으나(p<0.01), YGPDS 300 ㎍/㎖ 처리군에서는 1.59 ± 0.15배로 유의하게 억제되었다(p<0.01) (Fig. 6C).
따라서 YGPDS는 I-κBα의 인산화 및 분해를 막고, 결과적으로 NF-κB의 핵 내 이동을 차단함으로써 항염증 효능을 나타내는 것으로 판단된다.
NF-κB 경로 외에도 염증 반응에 관여하는 MAPK 경로(p38, ERK, JNK)의 인산화 변화를 확인하였다. LPS 단독 처리는 대조군에 비해 p38과 ERK의 인산화를 각각 2.19 ± 0.12배, 1.65 ± 0.17배로 유의하게 증가시켰다(p<0.01). 그러나 YGPDS 전처리군은 p38과 ERK의 인산화에 대해 통계적으로 유의미한 억제 효과를 나타내지 않았다 (Figures 7A, 7B, 7C).
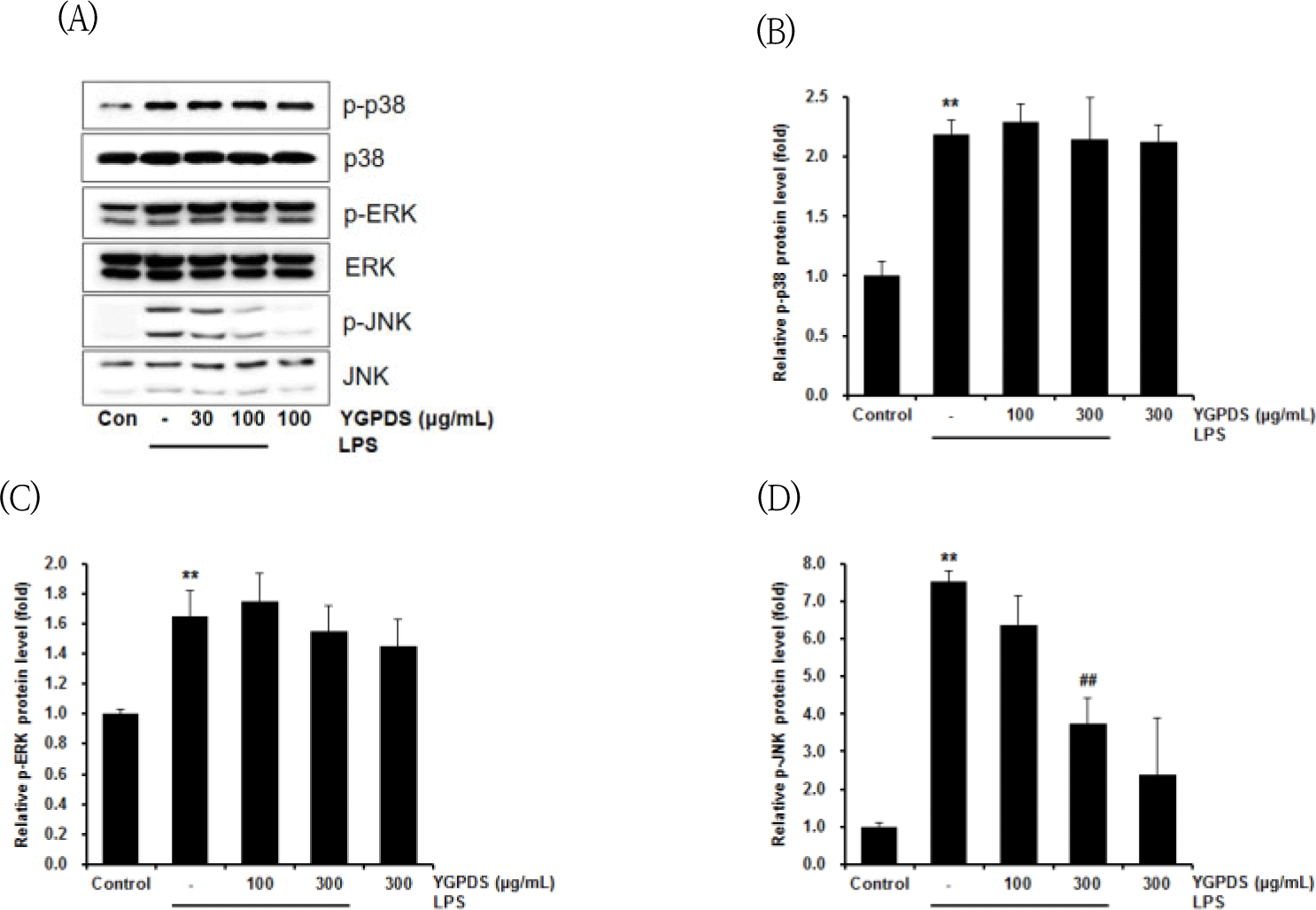
반면, JNK의 인산화는 LPS 처리에 의해 대조군 대비 7.51 ± 0.28배로 급격히 증가하였으나(p<0.01), YGPDS 300 ㎍/㎖ 처리군에서는 3.75 ± 0.69배로 나타나 LPS군 대비 유의하게 억제되었다(p<0.01) (Fig. 7A, 7D).
결론적으로 YGPDS는 MAPK의 하위 기전 중 p38이나 ERK가 아닌, 주로 JNK 경로를 선택적으로 억제함으로써 항염증 효과를 나타내는 것으로 판단된다.
Carrageenan(CA)으로 유도된 Rat 족부종 모델을 이용하여 YGPDS의 생체 내 항염증 효과를 평가하였다.
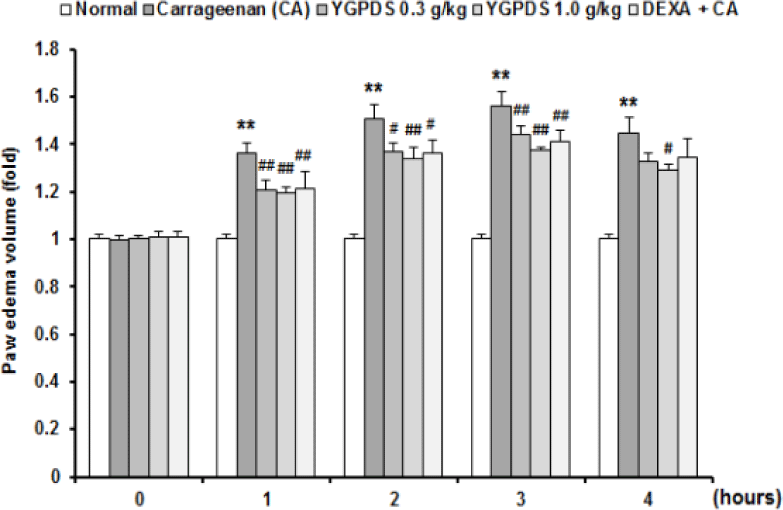
CA를 피하 주사한 대조군(Control)은 주사 후 시간이 경과함에 따라 족부종이 급격히 유발되었다. 상대적 족부피(Relative paw volume)는 1, 2, 3, 4시간 경과 시점에서 각각 1.36 ± 0.04, 1.51 ± 0.06, 1.56 ± 0.06, 1.45 ± 0.07 배로 나타나, 0시간(1.00 ± 0.02) 대비 모든 시간대에서 유의하게 증가하였다(p<0.01).
반면, YGPDS 투여군은 족부종을 농도 의존적으로 억제하였다. YGPDS 0.3 g/㎏ 투여군은 1, 2, 3시간 시점에서 대조군 대비 유의한 억제 효과를 나타내었다(p<0.05 또는 p<0.01). 특히 YGPDS 1.0 g/㎏ 투여군은 1, 2, 3, 4시간 시점에서 각각 1.20 ± 0.03, 1.34 ± 0.05, 1.37 ± 0.02, 1.29 ± 0.02 배를 기록하여, 모든 측정 시간대에서 대조군 대비 유의하게 족부종을 억제하였다((p<0.05 또는 p<0.01).양성 대조군인 Dexamethasone(1 ㎎/㎏) 투여군 역시 1, 2, 3시간 시점에서 유의한 부종 억제 효과를 보였으나(1.22 ∼ 1.41배), YGPDS 1.0 g/kg 투여군은 Dexamethasone 투여군과 유사하거나 수치적으로 더 우수한 부종 억제 효능을 나타내었다 (Fig. 8).
앞선 In vitro 실험에서 YGPDS가 iNOS 발현을 유의하게 억제함을 확인하였으므로, 실제 족부종 조직 내에서도 동일한 기전이 작용하는지 확인하였다.
족부종 유발 후 조직을 적출하여 iNOS 단백질 발현량을 분석한 결과, Carrageenan(CA) 투여군은 정상군(1.00 ± 0.37배) 대비 6.30 ± 0.33배로 iNOS 발현이 급격히 증가하였다(p<0.01).
YGPDS 0.3 g/㎏ 투여군에서는 5.36 ± 0.41배로 나타나 유의한 감소를 보이지 않았으나, 고농도인 YGPDS 1.0 g/㎏ 투여군에서는 3.65 ± 0.15배로 나타나 CA군 대비 유의하게 발현을 억제하였다(p<0.01) (Fig. 9).
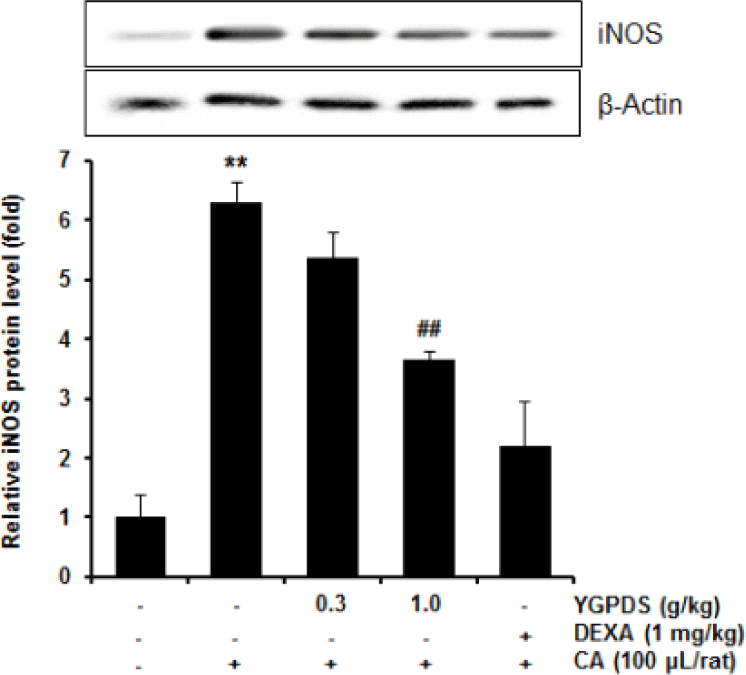
이는 YGPDS가 염증 부위 조직 내에서 iNOS 단백질의 과발현을 차단함으로써 부종을 완화시켰음을 시사한다.
족부종 모델에서 약물 투여에 따른 간 독성 발생 여부를 확인하기 위해 혈청 내 ALT 및 AST 활성을 측정하였다.
먼저 ALT 수치는 정상군(26.52 ± 0.96 IU/L)과 비교하여 CA군(24.20 ± 2.08 IU/L), YGPDS 0.3 g/㎏ 군(26.24 ± 0.69 IU/L), YGPDS 1.0 g/㎏ 군(26.51 ± 0.81 IU/L), Dexamethasone 군(28.18 ± 1.62$ IU/L) 간에 유의한 차이가 관찰되지 않았다 (Fig. 10A).
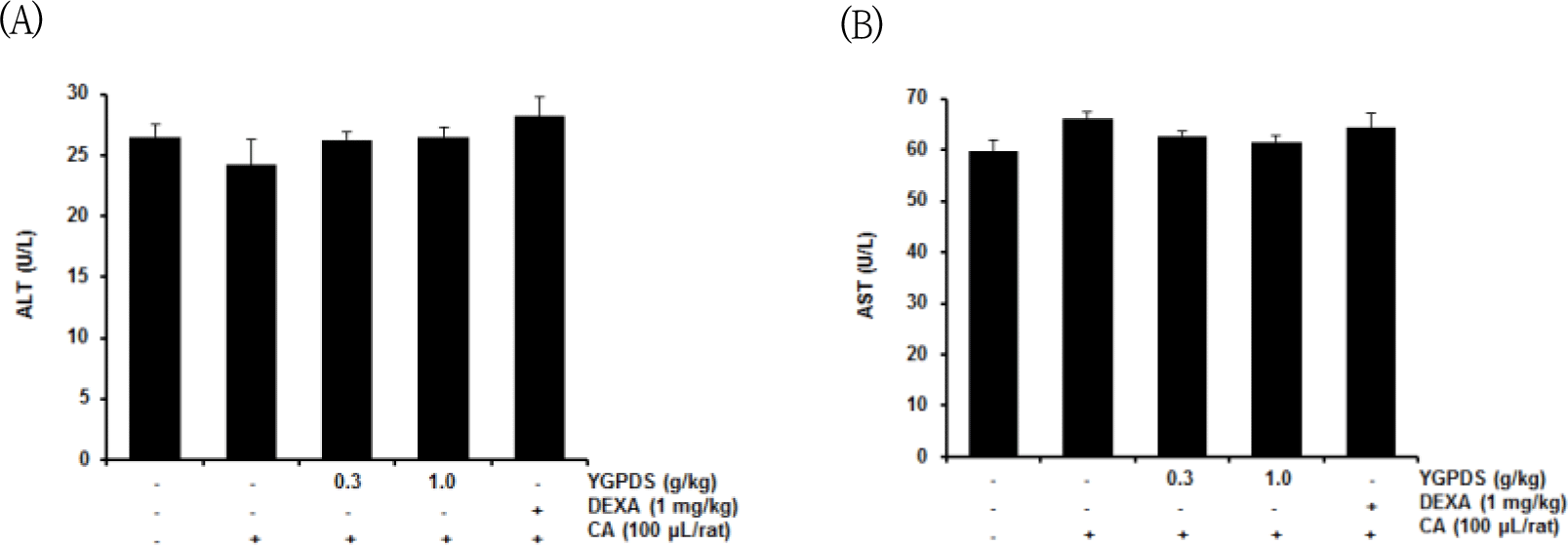
AST 수치 역시 정상군(59.71 ± 2.27 IU/L) 대비 CA군(66.11 ± 1.44 IU/L), YGPDS 0.3 g/㎏ 군(62.70 ± 0.93 IU/L), YGPDS 1.0 g/㎏ 군(61.61 ± 1.05 IU/L), Dexamethasone 군(64.32 ± 2.91 IU/L) 모두에서 유의한 변화가 없었다 (Fig. 10B).
따라서 본 실험에 사용된 YGPDS의 투여 용량(최대 1.0 g/㎏) 및 기간 내에서는 간 독성을 유발하지 않는 것으로 확인되었다.
Ⅳ. 고 찰
염증(Inflammation)은 생체 조직이 외부의 자극, 감염, 또는 손상에 대응하여 항상성을 유지하고 손상된 부위를 복구하려는 필수적인 방어 기전이다10). 그러나 이러한 방어 반응이 과도하게 발생하거나 지속될 경우, 정상 조직의 손상을 초래하고 만성적인 질환으로 이행될 수 있어 이를 적절히 제어하는 것은 임상적으로 매우 중요하다14-5). 한의학에서 發頤는 턱 부위, 즉 이하선에 발생하는 급성 화농성 연조직염을 의미하며, 현대 의학의 급성 화농성 이하선염이나 볼거리(Mumps)와 병리학적 유사성을 가진다. 이는 주로 熱病의 餘毒이나 수술 후 氣血이 쇠약해진 상태에서 毒邪가 침입하여 발생하며, 국소적인 발적, 부종, 심한 통증과 함께 개구장애 및 전신 발열을 동반하는 특징이 있다1). 이에 대한 치료는 급성 염증 반응을 신속히 억제하고 화농을 배출하며 조직의 부종을 감소시키는 淸熱解毒과 消腫散結이 중요하다16).
본 연구에서는 이러한 發頤 치료에 사용되어 온 《傷寒全生集》 連翹敗毒散(YGPDS)의 항염증 효능과 그 기전을 규명하고자 하였다. 본 처방의 구성 약물을 살며보면 YGPDS가 단순한 表證 치료제가 아님을 알 수 있다. 기존에 널리 연구된 《東醫寶鑑》의 連翹敗毒散은 荊防敗毒散을 기본으로 하여 주로 상기도 감염이나 초기 피부 질환과 같은 표재성 염증 질환에 응용되어 왔다4-7). 반면, 본 연구에서 주목한 《傷寒全生集》의 YGPDS는 獨活, 前胡, 荊芥 등 發散 위주의 약재를 제외하고, 梔子, 黃芩, 玄參과 같은 淸熱解毒 약재와 當歸, 芍藥, 紅花와 같은 活血散瘀 약재를 추가하거나 증량하였다. 梔子, 黃芩, 玄參은 심부의 熱毒을 직접적으로 제거하는 효능이 탁월하며, 當歸, 芍藥, 紅花는 염증으로 인한 국소 혈류 저체와 氣血瘀滯를 개선하여 조직의 회복을 촉진하고 통증을 완화하는 역할을 한다9). 이러한 구성의 변화는 염증이 심부 조직으로 파급되어 壅結된 상태, 즉 癰疽 및 發頤의 병리적 특성에 더욱 부합하는 것으로 판단된다. 실제로 본 연구의 UPLC 성분 분석 결과에서도 항염증 효과가 입증된 Baicalin, Forsythoside B, Geniposide 등이 다량 검출되어, 이러한 한의학적 配伍 원리가 실제 약리학적 성분 함량과도 밀접한 관련이 있음을 확인할 수 있었다.
대식세포를 이용한 In vitro 실험에서 YGPDS는 LPS 자극에 의한 염증 반응을 효과적으로 차단하였다. 대식세포는 그람 음성균의 내독소인 LPS에 노출되면 TLR4 수용체를 통해 활성화되며17), 이 과정에서 iNOS(inducible Nitric Oxide Synthase)가 과발현되어 다량의 NO(Nitric Oxide)를 생성한다. NO는 혈관 투과성을 증가시키고 부종을 유발하며 조직 손상을 가속화하는 주요 염증 매개 인자이다11). 본 실험에서 YGPDS는 세포 독성을 유발하지 않는 농도 범위에서 NO의 생성을 현저히 억제하였으며, 이는 iNOS 단백질의 발현 억제에 기인한 것임이 확인되었다. 이는 YGPDS가 염증 반응의 초기 단계에서 과도한 혈관 확장과 조직 손상을 방지할 수 있음을 의미한다.
나아가 YGPDS는 초기 염증 반응을 증폭시키는 전염증성 사이토카인(Pro-inflammatory cytokines)인 TNF-α, IL-6, IL-1β의 생성을 유의하게 억제하였다. TNF-α와 IL-6는 급성기 반응을 유도하고 발열 및 전신 증상을 초래하며, IL-1β는 염증의 만성화와 조직 파괴에 관여한다12). 또한, 본 연구에서는 케모카인인 MCP-1(Monocyte Chemoattractant Protein-1)의 억제 효과도 확인하였다. MCP-1은 혈액 내의 단핵구와 대식세포를 염증 부위로 유인하여 염증 반응을 가속화하고 혈관벽의 섬유화를 유발하는 인자이다13). YGPDS가 MCP-1의 생성을 억제한다는 것은 염증 세포의 추가적인 유입과 확산을 차단하여 염증의 순환 고리를 끊을 수 있음을 시사하며, 이는 發頤와 같이 급격하게 진행되는 심부 염증성 질환의 제어에 있어 매우 중요한 기전이라 할 수 있다.
이러한 다양한 염증 매개 인자들의 억제 효과는 분자적 수준에서 NF-κB 및 MAPK 신호 전달 경로의 조절을 통해 이루어지는 것으로 밝혀졌다. LPS가 대식세포의 TLR4에 결합하면 하위 신호 전달계를 통해 전사 인자인 NF-κB를 활성화시킨다. 평상시 세포질에 비활성 상태로 존재하는 NF-κB는 억제 단백질인 I-κBα와 결합해 있으나, 자극을 받으면 I-κBα가 인산화(p-I-κBα)되어 분해되고, 유리된 NF-κB가 핵 내로 이동하여 염증성 유전자의 전사를 촉진하게 된다12).
본 연구 결과, YGPDS 처리는 I-κBα의 인산화와 분해를 억제하여 세포질 내 I-κBα의 단백질 수준을 유지시켰으며, 결과적으로 NF-κB의 핵 내 이동과 활성화를 차단하였다. 또한, NF-κB와 함께 염증 신호를 전달하는 MAPK(Mitogen-Activated Protein Kinase) 경로에 대해서도 조절 작용을 보였다. MAPK 경로는 p38, ERK, JNK로 구성되는데12), YGPDS는 이 중 JNK의 인산화를 선택적으로 억제하는 것으로 나타났다. 이는 YGPDS가 광범위한 신호 차단보다는 특정 경로, 즉 NF-κB 및 JNK 경로를 표적으로 하여 효율적이고 특이적인 항염증 효능을 발휘함을 시사한다.
In vitro에서 규명된 항염증 기전이 실제 생체 내(In vivo)에서도 유효한지 확인하기 위해 Carrageenan 유발 족부종(Paw edema) 모델을 이용하였다. Carrageenan을 피하 주사하면 급성 염증 반응으로 인해 혈관 투과성이 항진되고 체액과 백혈구가 조직으로 침윤되어 부종이 발생한다18-9). 이는 임상적으로 癰疽나 發頤 환자에서 나타나는 급성 부종 및 종창과 유사한 병태 생리를 가진다. 실험 결과, YGPDS 투여군은 부종 유발 1시간 후부터 4시간까지 지속적이고 유의한 부종 억제 효과를 나타내었다. 특히 고용량(1.0 g/㎏) 투여군은 임상에서 항염증제로 사용되는 스테로이드 제제인 Dexamethasone 투여군과 비교했을 때, 초기부터 후기까지 대등하거나 더 우수한 부종 억제 효능을 보였다. 또한, 실험 종료 후 족부종 조직 내의 iNOS 단백질 발현을 측정한 결과, YGPDS 투여군에서 그 발현이 유의하게 감소하였다. 이는 YGPDS가 실제 염증 조직 내에서도 iNOS의 발현을 억제하여 NO 생성을 차단하고, 이를 통해 혈관 투과성 항진과 조직 부종을 완화시킴을 직접적으로 증명하는 결과이다. 즉, 세포 실험에서 확인된 분자적 기전이 생체 내에서도 그대로 구현되어 치료적 효과로 이어짐을 확인할 수 있었다.
마지막으로 약물의 장기간 복용 시 우려될 수 있는 간 독성 여부를 평가하였다. 간은 약물 대사의 주요 장기이며, 한약재의 안전성 논란에서 가장 중요하게 다루어지는 지표이다. 본 연구에서 YGPDS를 투여한 모든 실험군의 혈청 ALT 및 AST 수치는 정상군과 비교하여 유의한 차이를 보이지 않았다. 이는 본 실험에 사용된 고용량(1.0 g/㎏) 및 투여 기간 내에서 YGPDS가 간세포 손상을 유발하지 않으며, 임상적으로 안전하게 적용될 수 있음을 시사한다.
종합해 볼 때, 《傷寒全生集》의 YGPDS는 淸熱解毒과 活血散瘀의 약물 구성을 통해 급성 화농성 염증 질환에 특화된 효능을 발휘하는 것으로 판단된다.
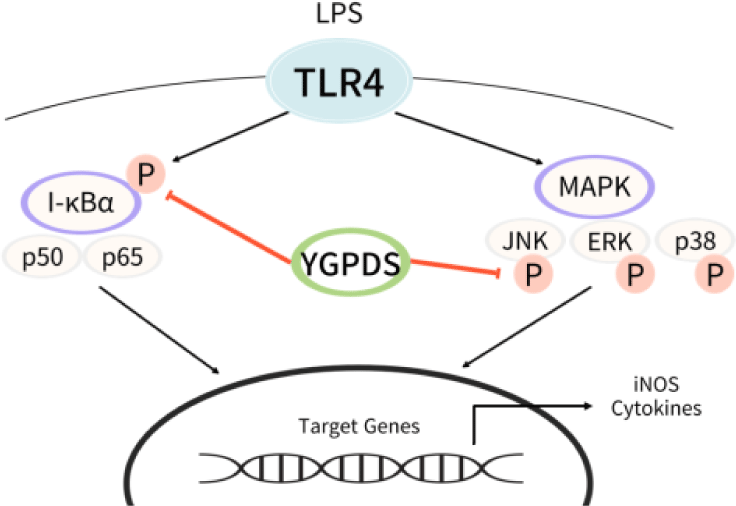
본 연구는 YGPDS가 대식세포 내 NF-κB 및 JNK 신호 전달 경로를 차단하여 NO, Pro-inflammatory Cytokines, Chemokine 등 다각적인 염증 매개 인자의 생성을 억제함을 규명하였다(Fig. 11). 또한, 동물 모델을 통해 이러한 기전이 실제 생체 내에서 강력한 부종 억제 효과로 발현됨을 입증하였으며, 간 독성에 대한 안전성 또한 확인하였다. 이는 YGPDS의 發頤 치료 효능을 분자생물학적 기전과 동물 실험을 통해 과학적으로 검증하였다는 데 큰 의의가 있다. 특히, 기존 《東醫寶鑑》 처방과 차별화된 염증 치료 효능에 대한 약리학적 근거를 마련함으로써, 향후 發頤와 같은 頭顏面部 급성 화농성 질환뿐만 아니라, 유사한 병리 기전을 가진 만성 타액선염이나 재발성 癰瘡 등 난치성 염증 질환 치료제로서 YGPDS의 임상적 활용 범위를 확대하는 데 기여할 것으로 사료된다.
Ⅴ. 결 론
본 연구에서는 連翹敗毒散(YGPDS)의 항염증 효능과 작용 기전을 규명하기 위해, LPS로 유도된 RAW 264.7 대식세포 모델과 Carrageenan으로 유발된 Rat 족부종 모델을 이용하여 실험을 진행하였다. YGPDS의 성분 분석, 염증 매개 물질 억제 효능, 세포 내 신호 전달 경로 조절 및 생체 내 부종 억제 효과를 종합적으로 분석한 결과, 다음과 같은 결론을 얻었다.
-
UPLC를 이용한 성분 분석 결과, YGPDS에는 항염증 효능이 알려진 Baicalin, Forsythoside B, Geniposide 등이 주요 지표 성분으로 함유되어 있음을 확인하였다.
-
세포 독성 및 NO 생성 억제 실험에서, YGPDS는 세포 생존율에 영향을 미치지 않는 농도 범위(30~300 ㎍/㎖)에서 LPS에 의한 NO 생성을 유의하게 감소시켰으며, 이는 iNOS 단백질의 발현 억제에 기인함을 확인하였다.
-
염증 매개 물질 제어 실험에서, YGPDS는 초기 염증 반응을 주도하는 전염증성 사이토카인인 TNF-α, IL-6, IL-1β와 염증 세포를 유인하는 케모카인인 MCP-1의 생성을 유의하게 억제하였다.
-
기전 연구 결과, YGPDS는 대식세포 내에서 I-κBα의 인산화 및 분해를 막아 NF-κB의 핵 내 이동을 차단하였으며, MAPK 신호 전달 경로 중 특히 JNK의 인산화를 선택적으로 억제함으로써 항염증 기전을 나타내었다.
-
족부종 실험에서, YGPDS 투여군(1.0 g/㎏)은 양성 대조군인 Dexamethasone과 대등한 수준의 부종 억제 효능을 보였으며, 실제 염증 조직 내에서도 iNOS 단백질의 발현을 유의하게 억제하였다.
-
안전성 평가에서, YGPDS를 투여한 모든 실험군에서 간 손상 지표인 혈청 ALT 및 AST 수치는 정상군과 유의한 차이를 보이지 않아, 생체 내에서의 간 독성에 대한 안전성을 확인하였다.
이상의 결과를 종합할 때, 連翹敗毒散(YGPDS)은 NF-κB 및 JNK 신호 전달 경로를 조절하여 다양한 염증 매개 인자의 생성을 차단하고, 실제 생체 내에서 강력한 부종 억제 효과와 안전성을 나타내었다. 이는 YGPDS가 發頤를 비롯한 급성 화농성 염증 질환 치료에 유의한 효능이 있음을 시사하며, 향후 관련 염증 질환 치료제로서의 임상적 활용 가치가 높을 것으로 사료된다.






