Ⅰ. 서 론
건선은 표피 각질세포의 과증식과 면역세포 활성화, 피부장벽 이상이 복합적으로 작용하는 만성 재발성 피부질환으로1) 대사증후군, 심혈관질환 등 다양한 전신 질환과 연관된 염증 질환으로 인식되고 있으며, 전 세계 인구의 약 2-3%가 이환되어 있다2,3).
건선의 치료에는 국소제, 광선요법, 면역억제제, 생물학적 제제가 사용되며, TNF-α, IL-17, IL-23 억제제가 대표적이다4). 그러나 장기 사용 시 감염이나 악성종양 등의 부작용이 있어서 상대적으로 안전한 치료제에 대한 필요성이 점차 강조되고 있다5,6).
한의학에서는 건선을 白疕·銀屑이라 하고, 血熱, 血燥, 血瘀 등의 병인에 따라 淸熱涼血·養血潤燥·活血祛瘀의 치법을 적용해 왔다7,8). 최근에는 이러한 한의학적 병리 개념이 IL-17 및 TNF-α 중심 염증 기전과 상관성이 있다는 해석도 제시되고 있어, 천연물 기반 치료 후보 탐색의 이론적 배경을 제공한다9).
木通(Akebia quinata, AQ)은 으름덩굴과에 속하는 낙엽 활엽 덩굴식물로, triterpenoid saponinns, flavonoid 등이 주요성분이며 이뇨, 소염, 진통, 淸熱利濕의 효능이 있다10,11). 기존의 木通 관련 연구로는 항염증, 항산화, 항노화, 항암, 심혈관 보호, 간 재생, 신경 보호, 진통 효과와 고지방식이 모델에서 지질대사 개선 효과 등이 있다10,12-15). 그러나 이런 광범위한 효능에도 불구하고 건선과 연관된 피부 염증 조절, 각질세포 증식 억제, 건선 피부염 개선 효과를 평가한 연구는 아직까지 접하지 못하였다.
이에 본 연구에서는 IMQ-유도 건선 피부염 모델에 木通 추출물을 사용하여, 피부 염증 반응과 각질세포 증식 이상의 건선에서 관찰되는 주요 표현형들을 중심으로 효능을 평가하였다. 그에 따라, 정상 인간 진피 섬유아세포(Normal Human Dermal Fibroblast, NHDF) 및 JB6 세포 기반의 in vitro 염증·세포 변형 억제 실험, RAW 264.7 대식세포에서의 IL-6 및 TNF-α 조절 효과, Imiquimod(IMQ) 유도 마우스 건선 피부염 모델을 이용한 in vivo 효능 평가, H&E 및 Ki-67 면역조직화학 분석을 통한 표피 비후 및 세포증식 지표를 평가하여 유의한 결과를 얻었기에 이에 보고하는 바이다.
Ⅱ. 재료 및 방법
본 연구에 사용된 木通은 대한민국 경상북도 청송군에서 채취된 것으로, 시료는 한국한의학연구원 한약 표준 자원은행에서 표본 관능 감정(sensory authentication) 및 유전자 분석(gene authentication)을 통해 Akebia quinata 종으로 정확히 동정되었으며, 감별 시험서 및 유전자분석 인증서는 한약 표준 자원은행에서 발급된 확인서와 같이 규명되었다(Fig. 1, 2). 약용 부위는 줄기로서 주피를 제거한 부분이다. 채취 및 가공은 가을철에 줄기를 채취하여 잔가지를 제거한 후 그늘에서 충분히 건조하였다.


건조된 木通 시료에 중량 대비 약 10배의 증류수를 첨가하고, 3시간 동안 환류 추출을 수행하였다. 추출 후, 여과 및 농축 과정을 거쳐 동결 건조했으며, 최종 수득률은 12.72%로 확인되었다.
木通 시료에 중량 대비 약 10배의 70% 에탄올을 첨가하고 35 ± 1℃에서 1시간 동안 추출을 2회 반복하여 추출하였다. 추출된 용액은 여과 및 농축 과정을 거쳐 동결 건조하였으며, 최종 수득률은 10.43%였다.
AQW 및 AQE는 한국한의학연구원 한약자원연구센터의 한약 표준 자원은행(Herbal Medicine Resources Research Center, Korea Institute of Oriental Medicine, Naju, Korea) 으로부터 분양받아 사용하였으며, 수령 후에는 –20℃에 보관하였다. 실험 전 AQW는 증류수를 이용하여, 에탄올 추출물은 dimethyl sulfoxide(DMSO)를 이용하여 200㎎/㎖의 농도로 stock solution을 제조한 후–20℃에 보관하고, 최종 농도로 희석하여 사용하였다.
본 연구의 세포 배양에 필요한 minimum essential medium(MEM), Dulbecco’s modified Eagle medium(DMEM), Medium199, fetal bovine serum(FBS), penicillin/streptomycin (P/S), sodium pyruvate(SP), minimum essential medium non-essential amino acid(MEM NEAA), trypsin-EDTA는 Gibco(Grand Island, NY, USA)에서 구매하였으며, DMSO, basal medium eagle(BME), IMQ, clobetasol propionate는 Sigma-Aldrich, Inc.(St. Louis, MO, USA)에서 구매하였다. WST-8 Cell Viability Assay Kit는 Biomax(Seoul, Republic of Korea)에서, Multiskan SkyHigh Spectrophotometer는 ThermoScientific(Vantaa, Finland) 제품을 사용하였다. 실험에 사용된 모든 시약은 분석급 이상을 사용하였다.
본 연구에서는 정상 피부세포의 독성평가를 위해 NHDF를 사용하였으며, 12-O-tetradecanoylphorbol-13-acetate(TPA)로 유도되는 세포 변형 억제효과를 평가하기 위해 쥐의 상피 세포주인 JB6 Cl41 세포를, IMQ에 의한 염증반응 평가를 위해 쥐의 대식세포인 RAW 264.7 세포를 각각 사용하였다. NHDF 세포는 American Type Culture Collection(ATCC, Manassas, VA, USA)에서 구입하였으며, Medium 199과 DMEM 배지를 1:1 비율로 혼합하고, 10% FBS 및 1% P/S (100U/㎖) 을 첨가하여 37℃, 5% CO₂ 조건의 가습형 인큐베이터에서 배양하였다. JB6 Cl41 세포는 동일 기관에서 분양받아 사용하였으며, MEM 배지에 5% FBS, 1% P/S, 1× SP, 1× MEM NEAA를 첨가하여 동일한 조건에서 배양하였다. 모든 세포는 2–3일마다 신선한 배지로 교체하였으며, 세포 밀도가 약 80–90%에 도달하면 0.25% trypsin-EDTA 용액으로 분리하여 계대배양하였다. RAW 264.7 세포(ATCC)는 DMEM에 10% FBS와 1% P/S를 첨가하여 37℃, 5% CO₂ 조건에서 배양하였으며, 세포 밀도가 약 70–80%에 도달하면 세포 스크레이퍼를 이용해 부착세포를 부유시켜 계대배양하였다.
NHDF 세포에 대한 木通 추출물(AQW, AQE)의 세포독성은 WST-8 분석을 통해 평가하였다. NHDF 세포를 96-well plate에 5×10³cells/well로 분주한 후 24시간 동안 안정화시켰다. 이후 AQW 및 AQE를 0, 1.56, 3.13, 6.25, 12.5, 25, 50, 100 ㎍/㎖ 농도로 처리하였고, DMSO는 최종 농도가 0.1% 이하가 되도록 조정하였다. 24시간 및 48시간 배양 후, 각 well에 Quanti-MAX WST-8 Cell viability Assay Kit reagent(Biomax, Seoul, Republic of Korea) 10㎕를 첨가하고 37℃에서 4시간 반응시켰다. Multiskan SkyHigh Spectrophotometer(ThermoScientific, Vantaa, Finland)를 이용하여 450㎚에서 흡광도를 측정하여 대조군 대비 세포 생존율을 산출하였다. 木通 추출물이 정상 세포에 미치는 독성 여부를 확인한 후, 비독성 농도를 이후 실험에 사용하였다.
JB6 Cl41 세포의 TPA 유도 세포 변형 억제효과는 Soft agar assay를 통해 평가하였다16). 하부층은 0.5% agar, MEM, 10% FBS, 2 mM L-glutamine, 5㎍/㎖ gentamicin을 혼합하고, 여기에 TPA(10ng/㎖) 및 AQE(0, 25, 50, 100 ㎍/㎖) 또는 AQW(0, 6.25, 12.5, 25 ㎍/㎖)을 각각 농도별로 첨가하여 6-well plate에 3㎖씩 분주하였다. 하부층은 상온에서 완전히 굳힌 후 다음 단계로 진행하였다. 상부층은 0.3% agar, MEM, 10% FBS, 2mM L-glutamine, TPA(10ng/㎖), 그리고 동일 농도의 AQE 또는 AQW를 포함하였으며, 여기에 JB6 C141 세포(8× 10³cells/well)를 혼합하여 하부층 위에 1㎖씩 분주하였다. Plate는 37℃, 5% CO₂ 조건의 가습형 인큐베이터에서 14일간 배양하였다. 형성된 colony는 광학현미경으로 관찰했으며, Image-Pro Plus software (v.6.0) program (Media Cybernetics, Silver Spring, MD, USA)을 사용하여 colony를 계수하였다.
본 실험은 木通 추출물(AQE, AQW)이 IMQ에 의해 유도되는 염증성 사이토카인 분비에 미치는 영향을 확인하기 위하여, RAW 264.7 대식세포를 이용하여 수행하였다. IMQ는 DMSO에 용해하여 stock 용액(10㎎/㎖)을 제조한 후, 실험 직전에 완전 배지로 희석하여 사용하였다. 木通 추출물은 AQE와 AQW로 구분하여 적용하였으며, 최종 DMSO 농도는 모든 처리군에서 0.1% 이하로 유지하였다. 추출물의 세포독성을 평가하기 위해, IMQ를 처리하지 않은 조건에서 AQE(1.25–100㎍/㎖) 및 AQW(1.25–100㎍/㎖)를 RAW 264.7 세포에 24, 48시간 단독 처리하였다. 이후 WST-8 Cell Viability Assay(Biomax, Seoul, Korea)를 수행하여 450㎚에서 흡광도를 측정하였다. Vehicle(0.1% DMSO) 처리군을 기준으로 생존율(%)을 계산하였다. RAW 264.7 세포는 6-well plate에 3×105cells/well로 분주하여 18시간 동안 안정화시켰다. 세포 안정화 후, RAW 264.7 세포에 AQE(50㎍/㎖) 또는 AQW(6.25㎍/㎖) 및 IMQ(5㎍/㎖)를 함께 처리하여 염증반응을 유도하였다. 자극 후 6시간에 세포 배양 상등액을 회수하여 cytokine 정량 분석에 사용하였다. IMQ 처리 후 회수한 상등액에서 염증성 사이토카인 TNF-α 및 IL-6의 농도는 상용 ELISA kit(LabisKoma, Seoul, Korea)의 지침에 따라 측정하였다. 흡광도는 450㎚에서 측정하였고, 표준곡선을 이용하여 농도를 산출하였다.
C57BL/6계통의 10주령 수컷 마우스(C57BL/6 male, 10 weeks old)를 샘타코 바이오코리아(Samtako Bio Korea, Osan, Korea)로부터 구입하여 실험에 사용하였다. 모든 동물은 온도 (22 ± 2℃), 습도 (55 ± 5%), 명암주기 (12h light/dark cycle) 조건이 유지되는 동물실험실에서 일주일간 적응시킨 후 실험에 사용하였으며, 사료와 물은 자유 급식·급수 조건으로 제공하였다. 모든 동물실험은 동신대학교 동물실험윤리위원회(Institutional Animal Care and Use Committee, IACUC) 의 승인(승인번호: DSU2025-05-02)을 받은 절차에 따라 수행되었다.
실험동물은 무작위로 9개 군으로 나누어 각 군당 6마리씩 배정하였다. 실험군은 다음과 같다:
-
① Vehicle 대조군,
-
② IMQ 단독 처리군(IMQ),
-
③ IMQ + Clobetasol 0.05% 처리군 (IMQ+Clobetasol),
-
④ IMQ + AQE 50㎎/㎏ 처리군(IMQ+AQE 50),
-
⑤ IMQ + AQE 100㎎/㎏ 처리군(IMQ+AQE 100),
-
⑥ IMQ + AQW 12.5㎎/㎏ 처리군(IMQ+AQW 12.5),
-
⑦ IMQ + AQW 25㎎/㎏ 처리군(IMQ+AQW 25)
-
⑧ AQE 100㎎/㎏ 단독 처리군(only AQE 100),
-
⑨ AQW 25㎎/㎏ 단독 처리군(only AQW 25).
모든 마우스는 IMQ 도포 4일 전에 등 부위의 털을 제모하여 피부를 노출시켰다. 건선 피부염(psoriasis dermatitis)은 등 부위에 Aldara 크림(5% IMQ, Ensign Laboratories Pty Ltd, Mulgrave, VIC, Australia)을 매일 6일간 도포하여 유도하였다.
木通 추출물 및 clobetasol propionate는 모두 아세톤에 희석하여 사용하였으며, 각각 200㎕의 용액을 등 부위에 균일하게 도포하였다. 木通 추출물 또는 clobetasol을 도포한 후 30분이 경과한 뒤 Aldara 크림 62.5㎎을 동일 부위에 도포하였다. 모든 처치는 매일 동일한 시간에 1회씩 실시하였으며, 총 6일간 반복하였다.
실험 종료 후 마우스를 안락사시킨 후, 등 부위의 피부조직을 절제하여 10% 중성 포르말린에 고정하였다. 고정된 조직은 Automatic tissue processor(Leica TP1020, Leica, Wetzlar, Germany)를 이용하여 70%, 80%, 90%, 95%, 100% 에탄올 순으로 각각 1시간씩 탈수(dehydration)하고, 이후 xylene 용액에서 3시간 투명화(clearing)한 뒤 파라핀에서 4시간 포매(paraffin embedding) 하였다. 파라핀 포매된 조직은 Paraffin Embedding Station(Leica EG1150 H, Leica, Wetzlar, Germany)으로 포매하여 블록을 제작하였으며, Rotary Microtome(HistoCore MULTICUT, Leica, Wetzlar, Germany)을 이용해 5㎛ 두께로 절편을 제작하였다. 제작된 절편은 55℃ 오븐에서 30분간 가열하여 파라핀을 연화시킨 후, xylene으로 5분씩 2회 처리하여 탈파라핀 하였다. 이후 100%, 95%, 70% 에탄올 순으로 재수화(rehydration) 후, hematoxylin과 eosin 용액을 이용하여 핵과 세포질을 차례로 염색하였다. 염색이 완료된 절편은 다시 저농도에서 고농도 에탄올을 거쳐 탈수하고, xylene으로 투명화한 후 슬라이드를 Permount mounting medium(Vector Laboratories, USA)으로 봉입하였다. 염색된 슬라이드는 PANNORAMIC Digital Slide Scanner(3DHISTECH Ltd., Budapest, Hungary)를 이용하여 20× 배율로 스캔하였으며, Slide Viewer 2.6 (3DHISTECH Ltd.) 프로그램을 사용해 조직학적 구조를 확대 관찰하였다. 표피 두께(epidermal thickness)는 Image-Pro Plus software(v.6.0, Media Cybernetics, Silver Spring, MD, USA)를 이용해 3군데의 임의 부위에서 측정하여 평균값으로 산출하였다.
55℃ 오븐에서 30분간 가열하고 xylene으로 2회 처리하여 파라핀을 제거하였다. 이후 100%, 95%, 70% 에탄올 순으로 재수화한 절편을 10mM sodium citrate buffer(pH 6.0)에 담가 가열하여 항원 복구(antigen retrieval)를 수행하였다. 충분히 식힌 뒤 1× PBS로 세척하였다. 내인성 과산화효소 활성을 제거하기 위해 3% H2O2 용액에 10분간 처리하였고, 이후 비특이적 결합을 차단하기 위해 10% normal goat serum (Gibco, USA)을 실온에서 30분간 처리하였다. 1차 항체로는 anti-Ki-67 antibody (1:200, Abcam, Cambridge, UK)를 사용하여 4℃에서 overnight 반응시켰으며, PBS로 세척한 후 HRP-conjugated secondary antibody(Vector Laboratories, USA)를 실온에서 1시간 반응시켰다. 발색은 DAB substrate(ImmPACT DAB, Vector Laboratories, USA)로 수행하였고, 핵 대조염색(counterstaining)은 Hematoxylin 용액으로 처리하였다. 염색이 완료된 절편은 탈수 및 투명화 과정을 거쳐 슬라이드를 봉입하였으며, PANNORAMIC Digital Slide Scanner(3DHISTECH Ltd., Budapest, Hungary)로 20× 배율에서 스캔하고 Slide Viewer 2.6 프로그램으로 확대 관찰하였다. Ki-67 발현은 갈색으로 염색된 핵을 기준으로 판정하였으며, Image-Pro Plus software (v.6.0)를 이용해 정량 분석하였다.
Ⅲ. 결 과
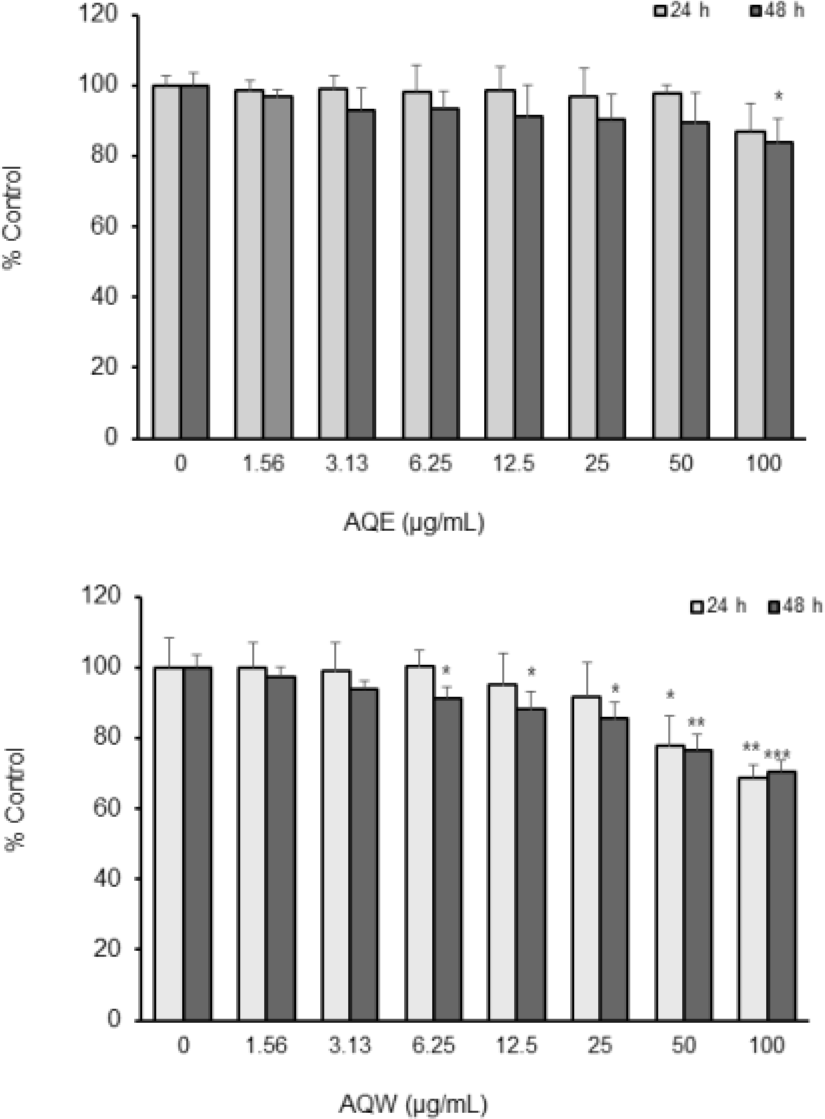
NHDF 세포에 AQE와 AQW를 각각 1.56–100 ㎍/㎖의 농도로 처리한 후, 24시간 및 48시간 배양 후 세포 생존율을 측정한 결과, 48시간 세포 생존율이 AQE는 100㎍/㎖까지, AQW는 25㎍/㎖까지 처리했을 때 80% 이상으로 유지되어 각각의 비독성 농도 범위를 확인하였다(Fig. 3).
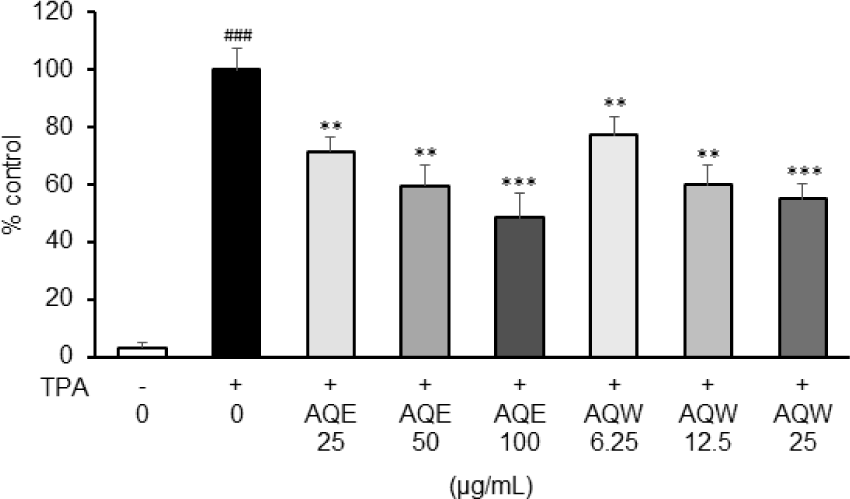
木通 추출물이 TPA에 의해 유도되는 JB6 Cl41 세포의 형태학적 변형을 억제하는지 평가하기 위해 soft agar assay를 수행한 결과, TPA(10ng/㎖) 처리군에서 JB6 C141 세포는 뚜렷한 colony 형성을 보였으나, AQE 및 AQW 처리군에서는 농도 의존적으로 colony 수와 크기가 유의하게 감소하였다(Fig. 4).

또, AQE 100㎍/㎖ 처리군에서 colony 형성 수는 TPA 단독군 대비 약 51.5% 이상 감소하였으며, AQW 25㎍/㎖ 처리군에서 45.0%가 감소하였다(Fig. 5).
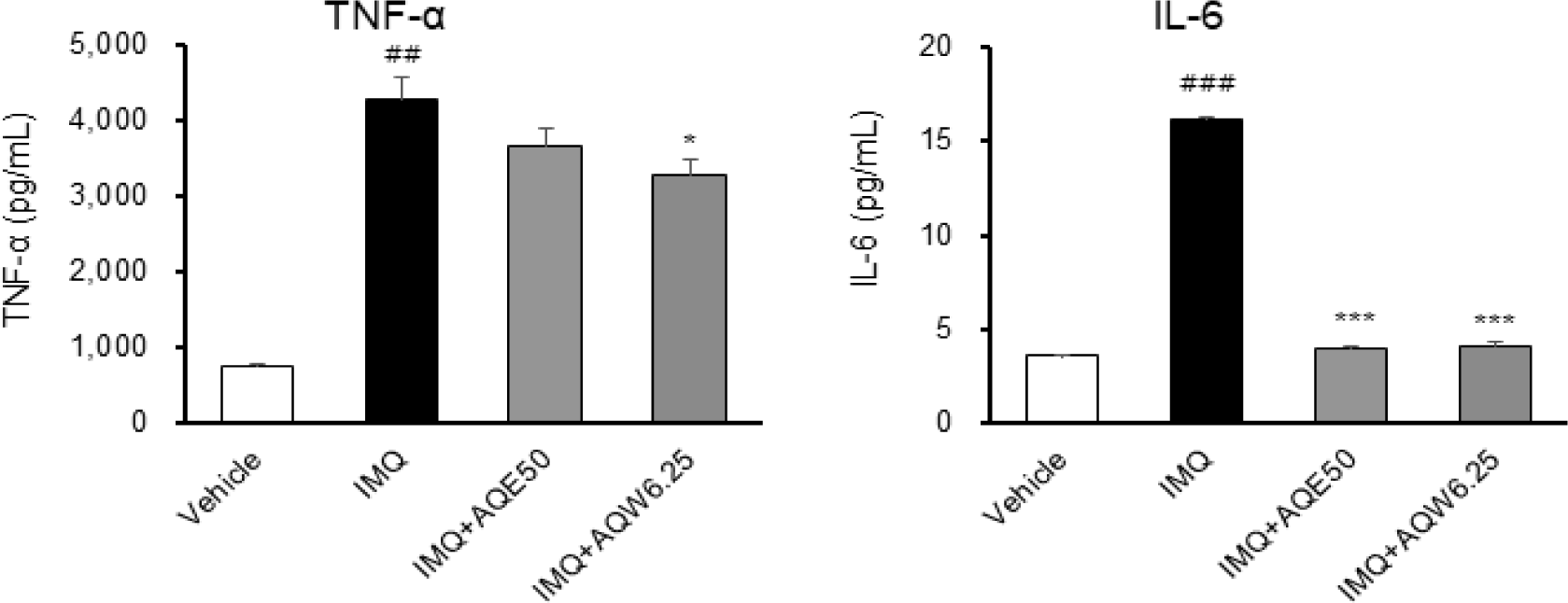
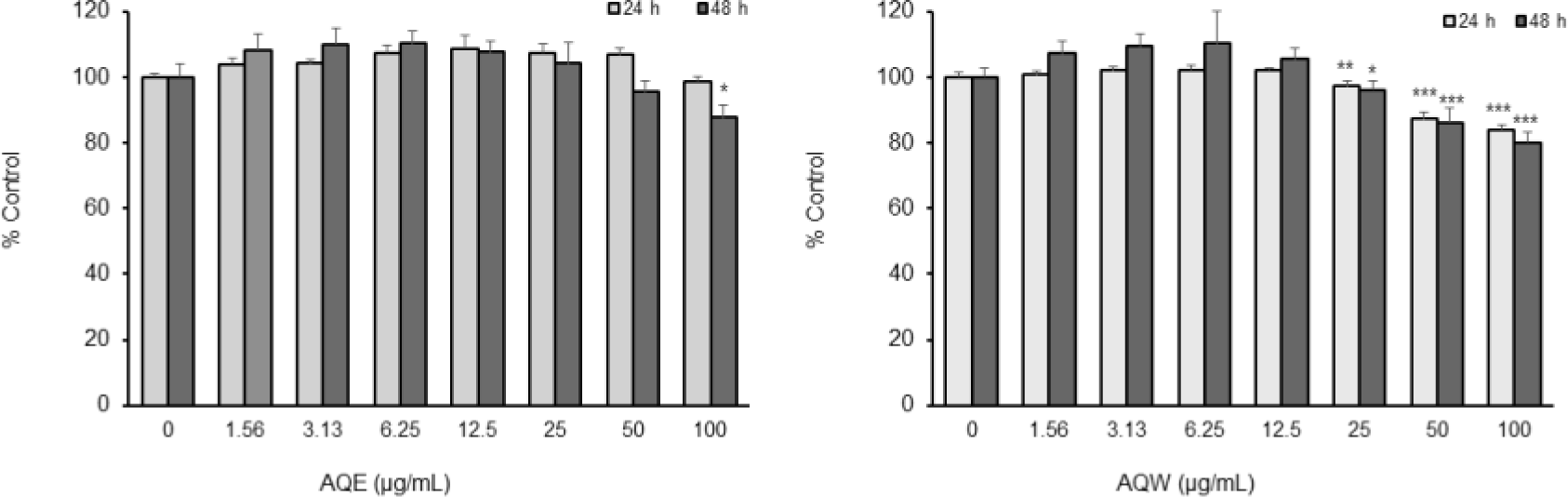
木通 추출물이 IMQ에 의해 유도되는 염증성 사이 토카인 분비 반응에 미치는 영향을 규명하기 위해 실험을 수행한 결과, RAW 264.7 대식세포에 IMQ (5㎍/㎖)를 처리하였을 때, 염증 매개 경로가 활성화되면서 TNF-α 및 IL-6의 분비가 6시간 처리 기준에서 유의하게 증가하였다(Fig. 6). RAW 264.7 세포에 IMQ와 함께 AQE(50㎍/㎖) 또는 AQW(6.25㎍/㎖) 를 처리하였을 때, 두 추출물 모두 IMQ-유도 TNF-α 및 IL-6 분비를 억제하였다. 한편 동일 조건에서 수행한 WST-8 세포 생존율 분석에서, AQE(25-100㎍/㎖) 및 AQW(6.25-25㎍/㎖) 처리 시 85% 이상의 생존율이 유지되었다(Fig. 7).
C57BL/6 수컷 마우스에 Aldara 크림(5% IMQ)을 등 부위에 6일간 도포하여 건선 피부염 모델을 유도하였다(Fig. 8A).
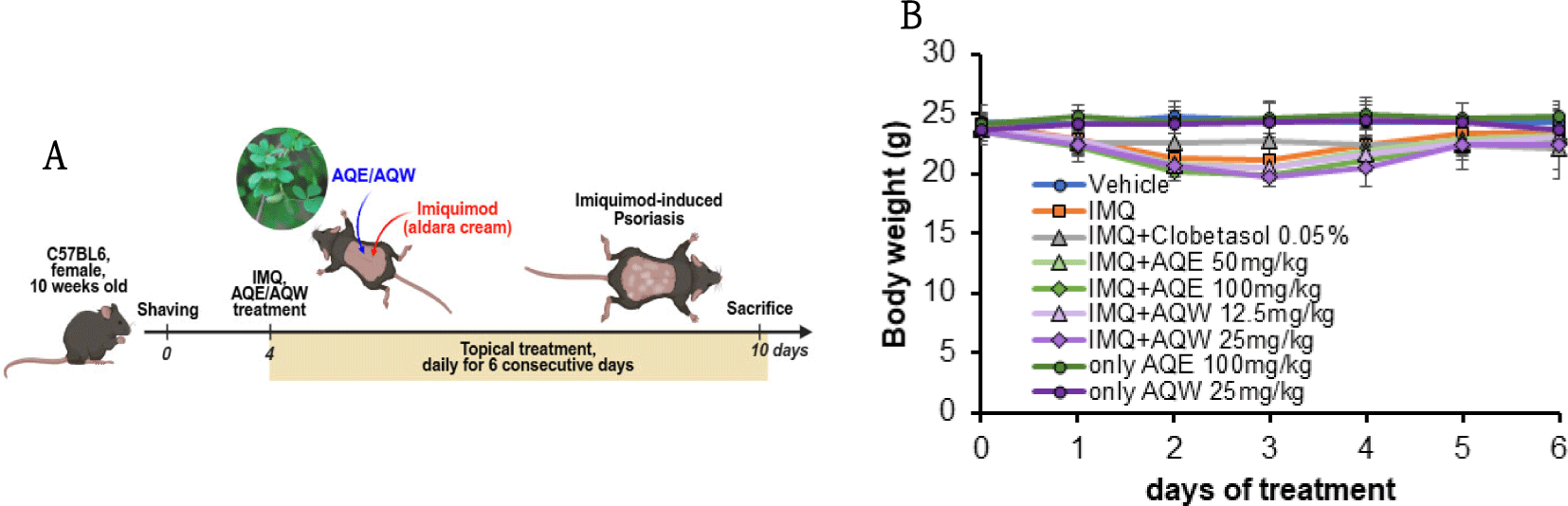
IMQ 처리 후 2–3일 차에 일시적인 체중 감소를 보 였으나, 4일차 이후부터는 점진적으로 회복되는 경향을 보였다. 반면, 木通 추출물(AQE 100㎎/㎏, AQW 25㎎/㎏) 단일 처리군에서는 실험 기간 동안 유의한 체중 감소가 관찰되지 않았다(Fig. 8B).
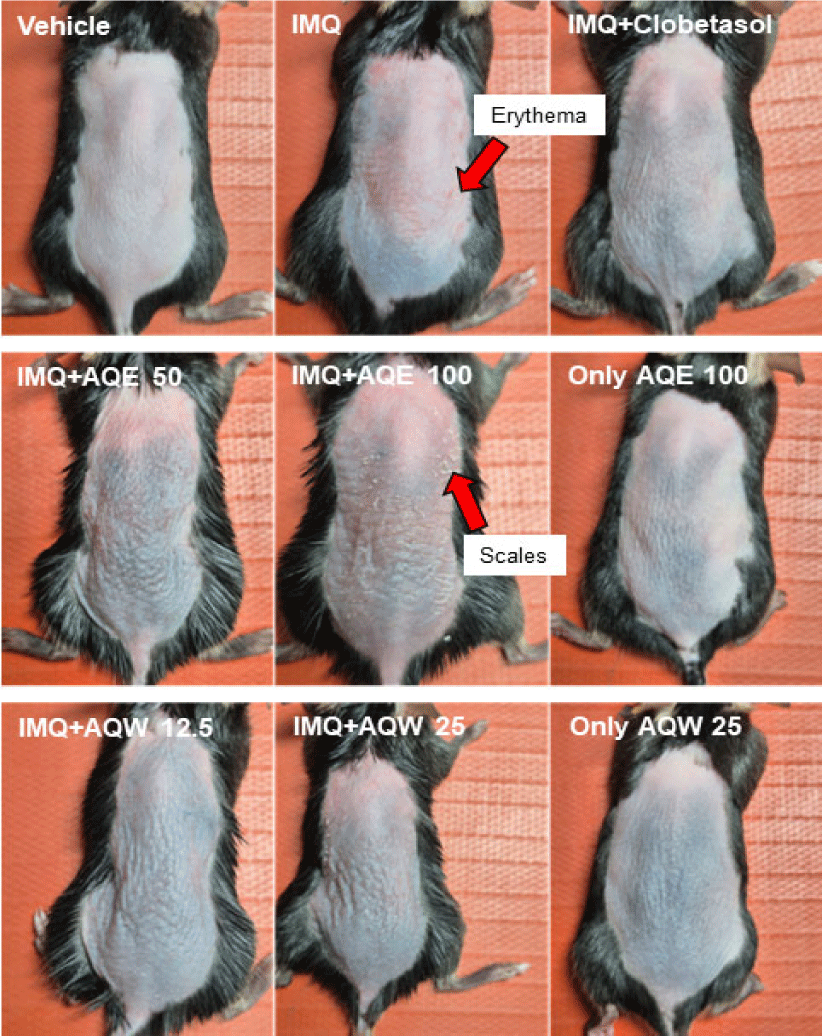
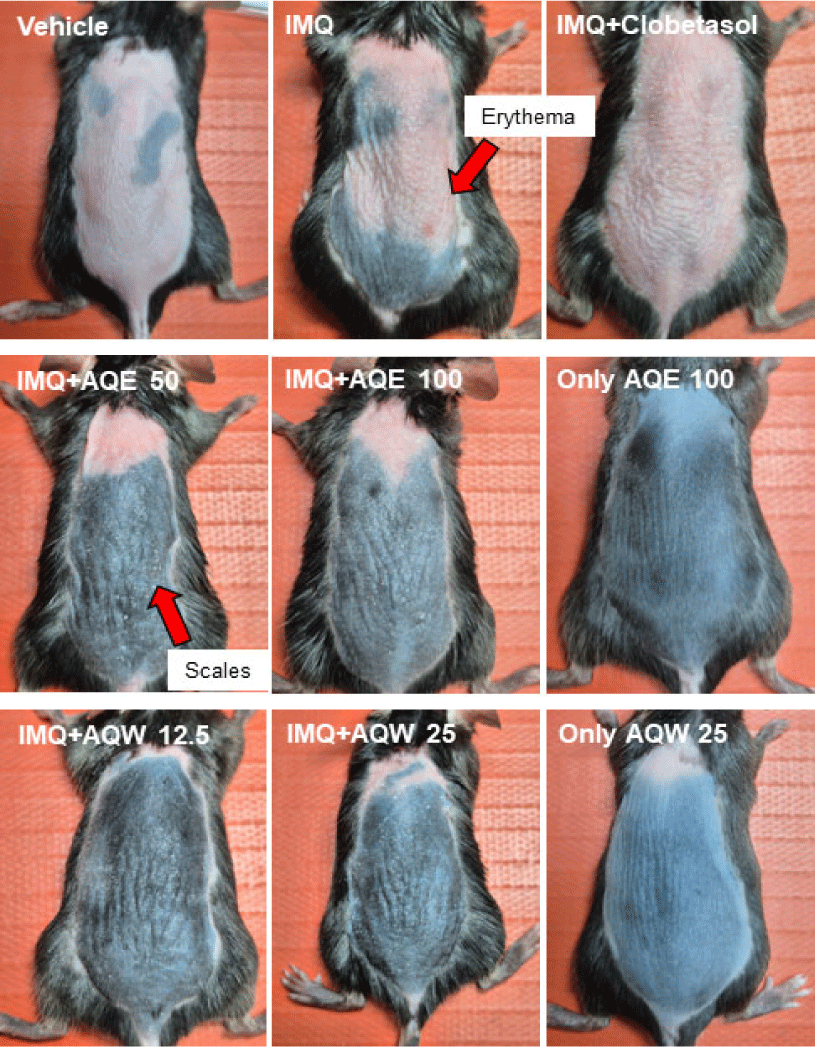
IMQ 단독 처리군에서는 도포 3일차부터 등 부위에 뚜렷한 홍반, 인설, 피부 비후가 관찰되었다(Fig. 9). 도포 6일차에는 병변 부위가 확대되어 전형적인 건선 피부염 양상이 나타났다 (Fig. 10). 이에 반해 木通 추출물(AQE, AQW) 처리군에서는 이러한 피부 병변이 완화되는 것을 확인하였다. 특히 AQW 12.5㎎/㎏ 처리군에서는 홍반과 인설이 가장 효과적으로 억제되었 으며, 피부 표면 상태가 Clobetasol 0.05% 처리군과 유사한 수준으로 회복되었다. AQE 처리군에서도 농도 의존적으로 증상이 완화되었으나, 그 효과는 AQW 12.5㎎/㎏ 처리군보다 다소 낮았다. AQE 또는 AQW 단독 처리군에서는 육안적 이상이 관찰되지 않았다(Fig. 10).
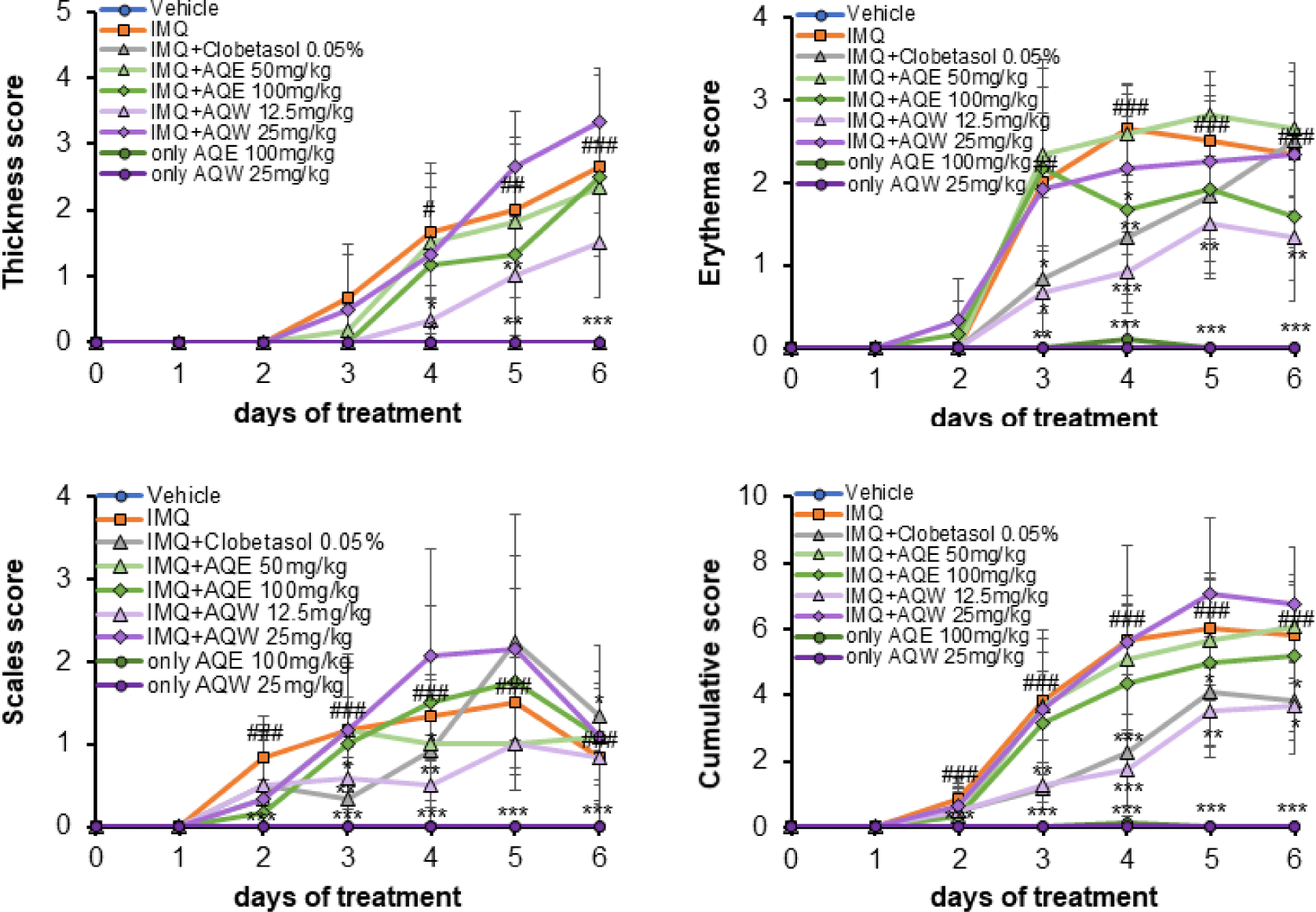
건선 병변의 정량적 지표로서 홍반, 인설, 피부 두께의 정도에 기초한 PASI-like 점수를 측정한 결과, IMQ 처리군은 투여 3일차부터 PASI 점수가 급격히 상승하여 5일차에 최대치에 도달하였다. 반면, AQE 및 AQW 처리군에서는 농도 의존적으로 PASI-like 점수가 감소하였다. 특히 AQW 12.5㎎/㎏ 처리군은 IMQ 단독군 대비 약 36.2% 이상의 감소를 보였으며, Clobetasol 0.05% 처리군과 유사한 수준으로 증상이 완화되었다. 한편, AQW 25㎎/㎏ 처리군에서는 피부 비후 및 인설 증가로 인해 PASI 유사 점수가 다소 상승하였으나, 통계적으로 유의한 차이는 관찰되지 않았다(Fig. 11).
H&E 염색 결과(Fig. 12, IMQ 단독 처리군) 에서는 표피층의 현저한 비후와 염증세포 침윤의 증가가 관찰되었다. 반면, AQE(50–100㎎/㎏) 및 AQW(12.5–25㎎/㎏) 처리군에서는 이러한 조직학적 변화가 눈에 띄게 완화되었으며, 특히 AQW 25㎎/㎏ 처리군에서는 표피층의 구조가 비교적 정상 형태를 유지하였다. Clobetasol 0.05% 처리군과 비교하여도 더 우수한 표피 보호 및 염증 억제 효과를 보였다.
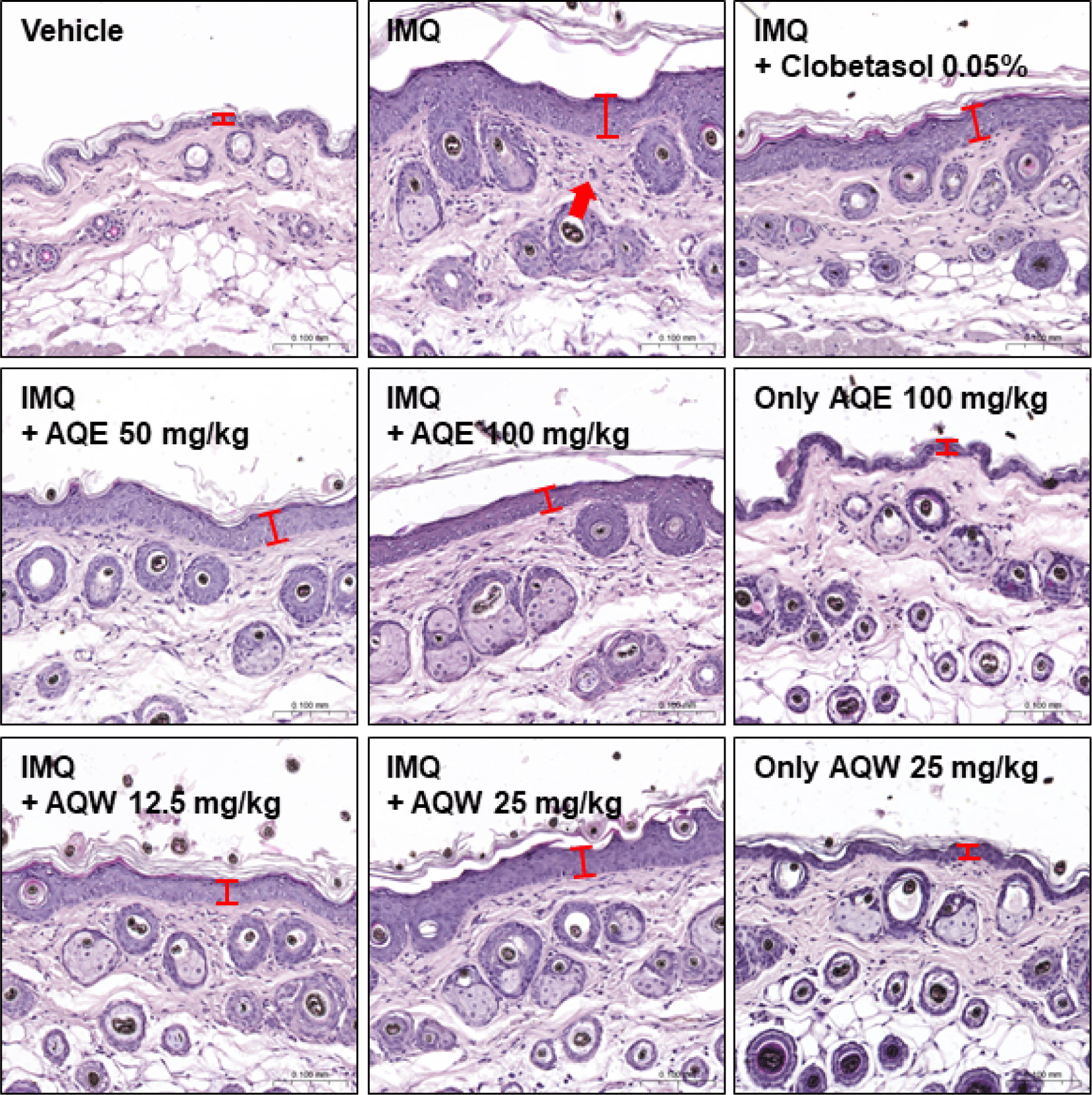
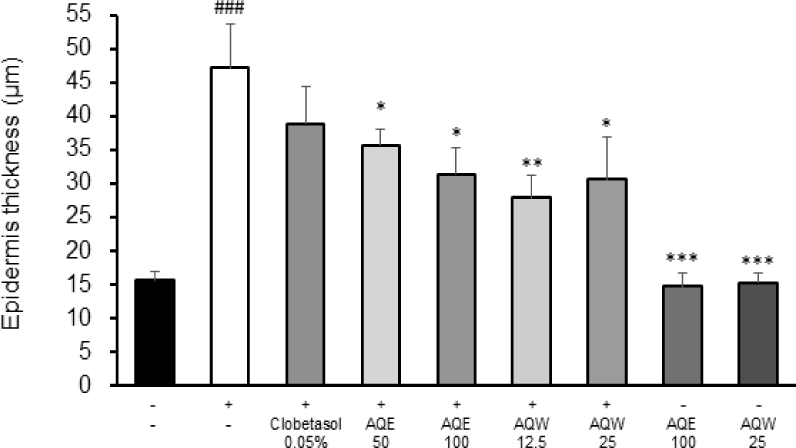
정량 분석 결과(Fig. 13), IMQ 단독 처리군의 평균 표피 두께는 47.2 ± 6.4㎛로 정상군(15.6 ± 1.2㎛)에 비하여 3배 정도 두꺼워졌으며, AQE 100㎎/㎏ 처리군의 평균 표피 두께는 IMQ군 대비 약 33.6% (p < 0.05), AQW 12.5㎎/㎏ 처리군에서는 40.9% (p < 0.01)의 유의한 두께 감소가 관찰되었다.
Ki-67 면역조직화학 염색 결과(Fig. 14)에 제시된 결과에서, IMQ 단독처리군은 표피층 전반에 걸쳐 Ki-67 발현이 관찰되었다. 반면, AQE(50, 100㎎/㎏) 및 AQW(12.5, 25㎎/㎏) 처리군에서는 Ki-67 발현이 현저히 감소하였으며, 특히 AQW 12.5㎎/㎏ 처리군에서 Ki-67 발현이 가장 억제된 양상을 보였다. Clobetasol 0.05% 처리군 또한 Ki-67 발현이 억제된 양상을 보였다 (p < 0.5).
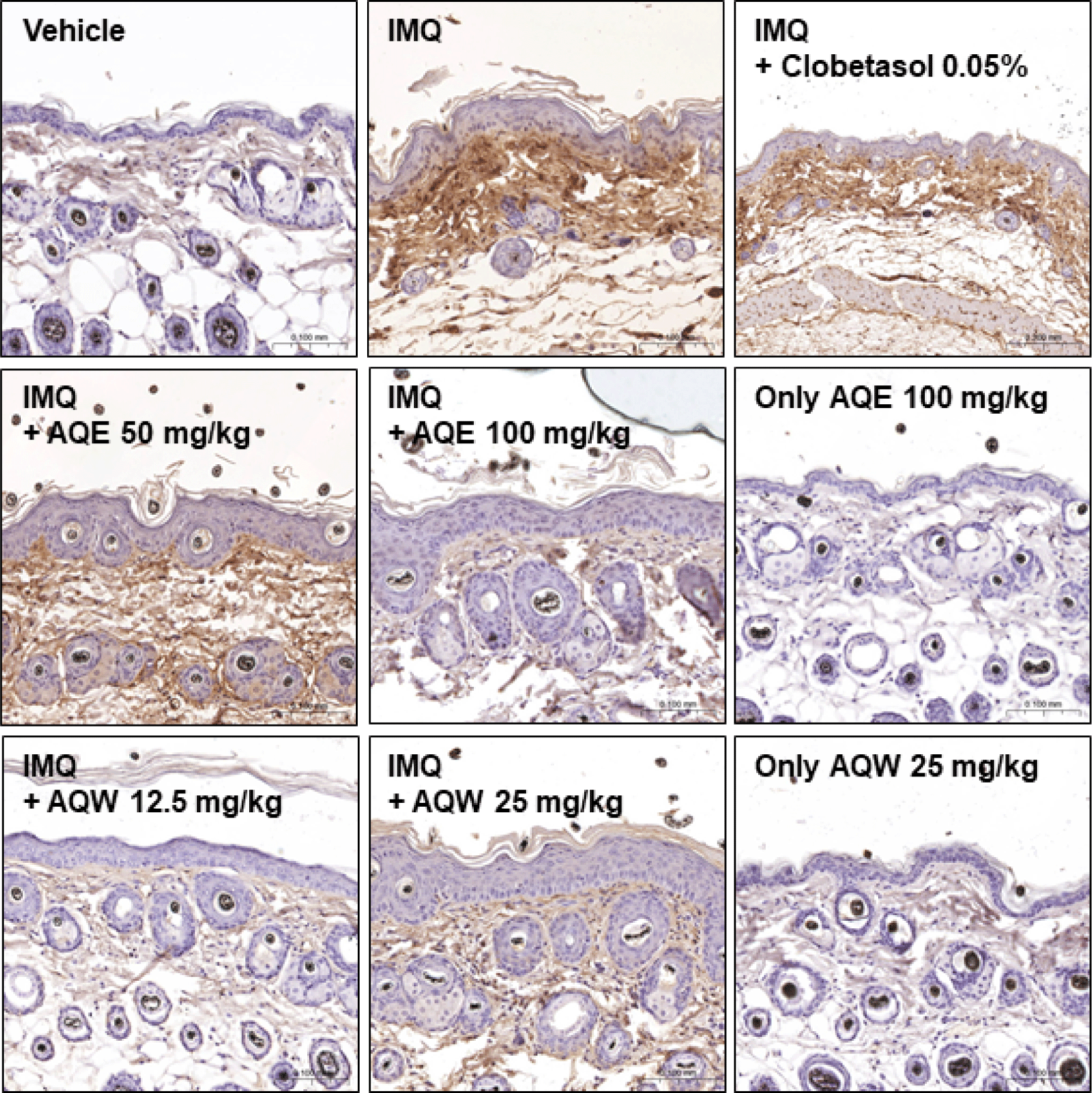
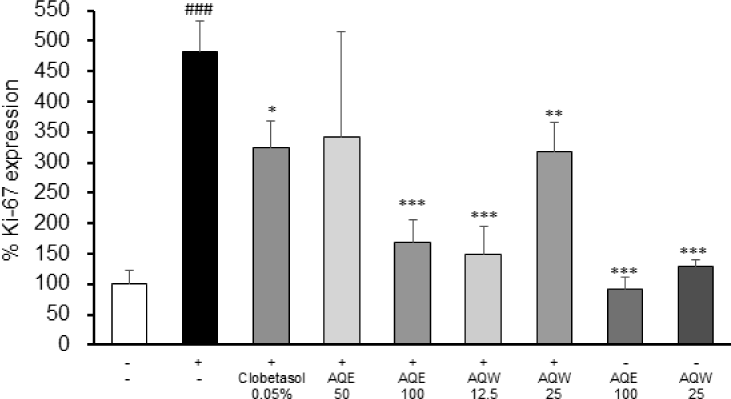
정량 분석 결과(Fig. 15), IMQ 군에서 Ki-67 발현 비율이 대조군 대비 약 4.8배 증가하였으나, AQE 100㎎/㎏군에서는 약 65.0% 이상 감소하였으며(p < 0.001), AQW 25㎎/㎏군에서도 약 69.0% 이상의 유의한 감소 경향이 확인되었다 (p < 0.001).
Ⅳ. 고 찰
건선은 만성 재발성 염증성 피부질환으로, 각질형성세포의 과증식과 면역세포의 과활성화, 염증성 사이토카인의 분비 증가가 특징이다1,2). 건선의 병태생리는 IL-23/IL-17 면역축(Th17 경로)의 과활성화와 NF-κB, JAK/STAT, MAPK 신호전달 이상으로 설명된다17,18). 이러한 염증 루프가 지속되면 각질세포의 증식과 염증반응이 악화되어 특징적인 홍반과 인설이 나타난다. 특히 IL-23/IL-17 면역축 은 건선 병리의 핵심 경로로 알려져 있으며, 이 경로는 선천면역세포(대식세포, 수지상세포 등)에서 분비되는 TNF-α, IL-6, IL-1β 등의 염증매개물이 상위 신호로 작용하여 활성화된다1,2,19-23).
최근 보고에 따르면, 전 세계적으로 건선의 유병률이 꾸준히 증가하고 있으며, 특히 고령층 인구 증가 및 환경적 요인으로 인해 향후 2030년까지 질병 부담이 지속적으로 상승할 것으로 예측된다24). 이러한 사회적 배경에서, 기존의 생물학적 제제나 스테로이드의 장기 사용에 따른 부작용을 보완할 수 있는 천연물 기 반 건선 치료제 개발의 필요성이 더욱 강조되고 있다5,6,25).
이에 따라, 염증 매개 인자를 조절하는 천연물 후보물질을 발굴하는 것은 건선 치료 연구에서 중요한 접근 전략으로 간주된다26,27). 실제로 많은 연구에서 천연 추출물이 항염증, 항증식, 항산화 특성을 가지고 있음이 밝혀졌다28-30). 이러한 증거들은 건선을 포함한 다양한 질병 치료에 천연물의 잠재적 유용성을 보여준다31-34).
한의학에서는 건선을 白疕·銀屑로 분류하고, 血熱, 血燥, 血瘀 등의 병인에 따라 淸熱涼血·養血潤燥·活血祛瘀의 치법을 적용해 왔다7,8). 이러한 전통적 병기는 현대 연구에서 제시하는 건선의 병태와 부합한다. 실제로 최근 보고된 생효탁리산(Sinhyotaklisan) 연구에서는 TNF-α, IL-6/IL-8, NF-κB, MAPK, VEGF-HIF-1α 경로가 건선 병태의 중심적 매개임이 확인되었으며, 다성분·다표적 접근이 psoriatic lesion의 염증, 증식, 혈관신생을 동시에 조절하는 데 유효함을 제시하였다35). 또한 건선과 대사증후군·지질대사의 밀접한 연관성을 조명한 연구에서는 혈중 LDL 증가, HDL 감소, 표피 지질 구조 이상 등이 전신 염증과 상호 강화되어 병변의 만성화를 촉진하여, 지질 대사 조절이 건선 치료의 새로운 축이 될 수 있음을 강조하였다36).
이러한 최신 근거들을 종합했을 때, 건선 치료에는 단일 병리를 표적으로 하는 접근보다는, 복합적인 병태를 동시에 조절할 수 있는 치료 전략이 필요함을 알 수 있다. 이러한 배경에서 木通은 피부에서의 항염증 효과뿐만 아니라 고지혈증 개선 효과도 보고된 바 있어, 본 연구에서는 우선 외용제로서의 가능성을 평가하고자 하였다12).
木通(Akebia quinata)은 으름덩굴과에 속하는 낙엽 활엽 덩굴식물로, 한의학에서 이뇨, 소염, 진통, 淸熱利濕 효능이 있는 약재로 활용되어 왔다10,11). 주요 생리활성 성분으로는 akeboside 계 triterpenoid saponins, hederagenin·oleanolic acid 기반 triterpenoids, 그리고 flavonoids 및 phenolic 구성물질이 풍부하게 포함되어 있으며11,37), 이들 중 akeboside St, hederagenin, oleanolic acid 등의 화합물은 항염증, 항산화, 항노화, 항암, 혈관이완 효과를 나타내는 것으로 알려져 있다38-40). 기존 연구에 따르면, 木通 추출물은 이뇨, 간 재생, 신경 보호, 진통, 항염증 및 항비만 효과를 나타낸다10,12-15).
그러나 木通을 건선과 같은 만성 염증성 피부질환에 적용한 연구는 보고된 바 없다. 木通이 지닌 항염증 및 항산화 활성이 피부 염증 반응과 세포 증식 이상이 복합적으로 얽혀 있는 건선 병태에 유효하게 작용할 가능성이 있다고 판단하였다. 이에 본 연구에서는 木通 추출물이 건선 관련 염증 및 표피 증식에 미치는 영향을 검증하고자 하였다.
먼저 NHDF에 대한 AQE와 AQW의 세포독성을 평가하기 위해 WST-8 assay를 수행하여 48시간 세포 생존율이 AQE는 100㎍/㎖까지, AQW는 25㎍/㎖까지 처리했을 때 80% 이상 생존율을 유지하여 기초 독성이 낮음을 확인하였다.(Fig. 3). 따라서 이후의 세포실험에서 AQE는 100㎍/㎖까지, AQW는 25㎍/㎖까지의 농도를 사용하였다.
또한, TPA로 유도된 JB6 C141 세포 변형 모델에서 형태학적 변형을 억제하는지 평가하기 위해 soft agar assay를 수행하였을 때, colony 형성을 농도 의존적으로 억제하였다(Fig 4). 이는 木通 추출물이 피부세포의 비정상적인 증식 및 변형 과정을 효과적으로 차단할 수 있음을 시사하며, 건선에서의 각질형성세포 과증식 및 조직 비후 억제 기전과 연결된다21). 특히 AQE 100㎍/㎖ 처리군에서 colony 형성 수는 TPA 단독군 대비 약 51.5% 이상 감소하였으며, AQW 25㎍/㎖ 처리군에서 45.0%가 감소하였다(Fig. 5). 이는 木通 추출물이 TPA-유도 세포 변형을 효과적으로 억제함을 의미한다.
대식세포주 RAW 264.7을 이용하여 木通 추출물의 IMQ(5㎍/㎖) 자극에 따른 염증성 사이토카인 분비 반응을 분석하였다. IMQ는 Toll-like receptor 7(TLR7) 을 자극하여 MyD88-의존성 NF-κB 및 MAPK 신호전달 경로를 활성화시키며, 이로 인해 TNF-α와 IL-6 같은 염증성 사이토카인이 급격히 분비된다22)(Fig. 6). 본 연구에서 AQE(50㎍/㎖) 및 AQW(6.25㎍/㎖) 처리 시, IMQ-유도 TNF-α 및 IL-6 분비가 억제되었고, WST-8 분석 결과 85% 이상의 세포 생존율이 유지되어 비독성 범위 내 효과임이 입증되었다(Fig 7). 이러한 결과는 木通 추출물이 대식세포에서 염증성 사이토카인 생성을 억제함으로써 in vitro 수준에서 항염 반응 조절 가능성을 보여주며, 이러한 면역세포 수준의 효과는 in vivo에서 관찰된 피부 염증 완화 및 세포 증식 억제와 직접적으로 연결된다.
이어, IMQ-유도 건선 피부염 마우스 모델을 통해 木通 추출물의 피부 병변 완화 및 세포 증식 억제 효과를 평가하였다. 이 모델은 사람의 건선 병태와 유사한 표피 비후, 인설 형성, 홍반, 면역세포 침윤 등을 재현하는 대표적인 동물모델이다. 본 실험은 제모 후 4일부터 6일간 木通 추출물(AQE, AQW) 및 Clobetasol 0.05%는 아세톤에 용해하여 동일 부위에 200㎕씩 도포하였으며, 30분 후 Aldara 크림을 매일 1회 도포하였다(Fig. 8A). IMQ 처리 후 보였던 일시적인 체중 감소는 4일 차 이후 점진적으로 회복되었다(Fig. 8B). 이는 IMQ 유도 염증 반응에 따른 일시적 스트레스 반응으로 해석된다. 반면, 木通 추출물(AQE, AQW) 단일 처리군에서는 체중 감소가 없었다(Fig. 8B). 이는 木通 추출물의 처리 농도에서 전신 독성이 유발되지 않았음을 시사한다. AQE 및 AQW를 처리한 군은 IMQ 단독군에 비해 피부 병변이 완화되는 것이 관찰되었다(Fig 9, Fig 10). 또, PASI-like 점수가 유의하게 감소하였다(Fig 11). 이는 木通 추출물이 IMQ-유도 건선 피부염의 임상적 증상(피부 염증 반응, 과각화)을 효과적으로 억제함을 입증한다.
木通 추출물(AQE, AQW)이 IMQ로 유도된 건선 피부염 모델에서 피부의 조직학적 변화를 완화할 수 있는지 평가하기 위한 H&E 염색의 결과 표피 비후가 현저히 완화되었다. 이는 木通 추출물(AQE, AQW)이 IMQ로 유도된 피부 염증 반응과 각질형성세포의 비정상적 증식으로 인한 표피 비후화를 효과적으로 억제함을 의미한다. 따라서 木通 추출물은 피부 세포의 과도한 증식을 조절하고 염증성 미세환경을 완화함으로써, 건선 피부염의 병리적 진행을 완화하는 조직학적 보호 효과를 갖는 것으로 판단된다.
Ki-67은 세포의 증식 활성을 대표하는 지표로, 건선 피부에서 과도하게 활성화된 각질형성세포의 증식 정도를 평가하는 주요 생체표지자로 알려져 있다. 본 연구에서는 IMQ로 유도된 건선 피부염 마우스 모델에서 木通 추출물(AQE, AQW)이 각질 형성세포의 증식 억제에 미치는 영향을 확인하기 위해 Ki-67 면역조직화학 염색(Immunohistochemistry, IHC)을 실시한 결과 각질형성세포의 증식 억제가 확인되었으며, 이는 木通 추출물이 IMQ로 유도된 피부세포의 비정상적인 증식 경로를 조절함으로써 건선 피부 병변의 진행을 완화할 수 있음을 시사한다. 따라서 木通 추출물은 건선 피부염의 병태생리에서 중요한 역할을 하는 세포 증식 조절 인자로 작용할 가능성이 있다. 특히 AQW(12.5㎎/㎏)에서 가장 우수한 개선 효과가 나타났는데, 이는 수용성 성분군(예: glycosylated triterpenoid saponins)의 생체 이용률 또는 피부 침투 특성이 AQE와 차이를 보였을 가능성이 있다. 이는 木通 추출물의 효능 차이가 단순 농도 문제가 아닌 추출 용매에 따른 활성 성분군의 차이와 관련될 수 있음을 시사한다.
본 연구에서의 실험 결과를 종합하면, 木通 추출물은 NHDF에서는 80% 이상의 세포 생존율이 유지되어 안전성이 확인되었으며, JB6 C141 세포에서는 TPA-유도 세포 변형이 농도의존적으로 억제되어 세포 수준의 항증식 효과가 입증되었다. 또한, 대식세포주 RAW 264.7에서는 IMQ 자극에 의해 유도된 TNF-α 및 IL-6 분비가 유의하게 감소하여, 염증성 사이토카인 생성을 조절함을 확인하였다. IMQ-유도 건선 피부염 마우스 모델에서도 표피 비후가 유의하게 완화되었으며, Ki-67 면역조직화학 염색에서 각질형성세포의 과증식이 감소하였다. 이러한 결과는 木通 추출물이 비정상적인 피부세포 증식 경로를 조절하여 건선 병변의 진행을 완화할 가능성을 보여준다. 다만 본 연구는 건선의 핵심 면역 기전을 직접 규명하기보다는, IMQ 자극으로 유도되는 피부 염증 반응과 각질형성세포 증식 이상이라는 건선에서 관찰되는 주요 표현형에 대한 항염 및 항증식 효과를 평가하는 데 초점을 두었다.
본 연구는 다음과 같은 제한점을 가진다. 첫째, IL-23·IL-17A/F·IL-22 등 Th17 축의 핵심 사이토카인 측정이 이루어지지 않아, 木通 추출물이 Th17 면역반응을 직접적으로 조절하는지는 추가 연구가 필요하다. 둘째, AQE·AQW 간 성분 차이에 대한 정량 분석(LC-MS, HPLC 등)이 수행되지 않아, 활성 기여 성분의 비교가 충분히 이루어지지 못했다. 셋째, 표피세포 자체에 대한 직접적 기전 연구가 부족하므로, NF-κB·MAPK·STAT3·Nrf2 등의 분자 신호 경로 분석이 후속적으로 필요하다. 넷째, 본 연구에서는 木通 추출물을 외용제로 적용하여 평가하였으므로, 한약의 일반적인 투여 방식인 경구 투여 조건에서의 약물동태학적 및 전신적 효과는 본 연구 범위에 포함되지 않았다.
향후에는 木通 추출물 내 주요 활성 성분(예: hederagenin, akeboside D 등)을 분리·동정하고, 세포 증식 관련 신호 경로 및 IL-23/IL-17 면역축에 대한 작용 가능성을 추가적으로 규명할 필요가 있다. 또한, 3D human skin equivalent 모델 및 전임상 연구를 통해 피부 침투율, 국소 안정성, 약물동태학적 특성을 규명한다면, 木通 추출물의 항건선 소재로서의 실질적 응용 가능성을 더욱 구체화할 수 있을 것이다.
Ⅴ. 결 론
-
AQE 및 AQW는 NHDF 세포에서 독성을 나타내지 않았으며, 세포 생존율 80% 이상으로 안전성이 확인되었다.
-
TPA로 유도한 JB6 Cl41 세포 변형 시험에서 AQE 및 AQW는 농도 의존적으로 세포 변형을 억제하여, 피부세포의 비정상적 증식 신호 차단 가능성을 보였다.
-
대식세포주 RAW 264.7 세포에서 수행한 ELISA 분석 결과, IMQ(5㎍/㎖) 자극에 의해 유의하게 증가한 TNF-α 및 IL-6 분비는 AQE(50㎍/㎏) 및 AQW(6.25㎍/㎏) 처리에 의해 감소하였다.
-
IMQ 유도 마우스 모델에서 AQW 12.5㎎/㎏군은 clobetasol 0.05%군과 유사한 수준으로 홍반, 인설, 표피 비후 등 건선 병변을 유의성 있게 완화하였다.
-
H&E 염색에서 AQE 및 AQW 처리군의 표피 비후가 감소하였다.
-
Ki-67 면역염색에서 AQE 및 AQW 처리군의 각질형성세포의 증식이 유의하게 억제되었다.






